题目内容
2.物质的量为0.10mol的镁条在足量的、且只含有CO2和O2混合气体的容器中充分燃烧(产物不含碳酸镁),反应后容器内固体物质的质量可能( )| A. | 2.2g | B. | 4.2g | C. | 4.4g | D. | 4.8g |
分析 若发生2Mg+CO2=2MgO+C时固体质量最大,若发生2Mg+O2=2MgO时固体质量最小,以此来解答.
解答 解:由2Mg+CO2=2MgO+C可知,0.1molMg完全反应时,生成固体的质量为0.1mol×40g/mol+0.05mol×12g/mol=4.6g,
由2Mg+O2=2MgO可知,0.1molMg完全反应时,生成固体的质量为0.1mol×40g/mol=4g,
因CO2和O2混合气体均与Mg反应,则反应后容器内固体物质的质量介于4g~4.6g之间,
故选BC.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应及极性法计算为解答的关键,侧重分析与计算能力的考查,注意极性法的应用,题目难度不大.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目
13.如图装置可以用来发生、洗涤、干燥、收集(不考虑尾气处理)气体.该装置可用于( )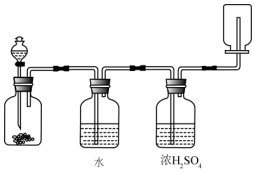

| A. | 锌和盐酸生成氢气 | B. | 氯酸钾和二氧化锰生成氧气 | ||
| C. | 碳酸钙和盐酸生成二氧化碳 | D. | 氯化钠和浓硫酸生成氯化氢 |
10.己知下列反应的离子方程式:
a.向NaHCO3溶液中滴加稀盐酸:HCO3-+H+=CO2↑+H2O
b.向NH4Cl溶液中滴加NaOH稀溶液:NH4++OH-=NH3•H2O
下列说法正确的是( )
a.向NaHCO3溶液中滴加稀盐酸:HCO3-+H+=CO2↑+H2O
b.向NH4Cl溶液中滴加NaOH稀溶液:NH4++OH-=NH3•H2O
下列说法正确的是( )
| A. | NaHCO3在水溶液中的电离方程式为NaHCO3=Na++H++CO32- | |
| B. | NaHCO3溶液与NaOH溶液反应的离子方程式为H++OH-=H2O | |
| C. | NH4NO3溶液与NaOH稀溶液反应的离子方程式为NH4++OH-=NH3•H2O | |
| D. | NH4NO3溶液与足量Ba(OH)2溶液反应的离子方程式为Ba2++CO32-=BaCO3↓ |
17.可以使用图如装置和指定试剂进行制备、干燥、收集的是( )
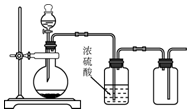

| A. | 用锌和稀硫酸制备H2 | B. | 用铜和稀硝酸制备NO | ||
| C. | 用30%H2O2水溶液和MnO2制备O2 | D. | 用MnO2和浓盐酸制备Cl2 |
7.Mg-AgCl电池是一种以海水为电解质溶液的水激活电池.下列叙述错误的是( )
| A. | 负极反应式为Mg-2e-═Mg2+ | |
| B. | 负极可能会发生副反应Mg+2H2O═Mg(OH)2+H2↑ | |
| C. | 电池放电时Cl-由负极向正极迁移 | |
| D. | 正极反应式为AgCl+e-═Ag+Cl- |
14.取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,标准状况下均产生5.6L气体,则两份铝片的质量之比为( )
| A. | 一定为1:1 | B. | 可能为2:3 | C. | 一定为3:2 | D. | 可能为1:6 |
11.水合碱式碳酸镁[4MgCO3•Mg(OH)2•4H2O〕,又称轻质碳酸镁.常利用菱镁矿(质量含量为碳酸镁90%,碳酸钙10%〕碳化法制取:
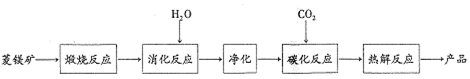
(1)根据下列表格数据,选择消化反应的最佳温度70℃;理由是温度进一步升高同等幅度,转化率几乎不变,但能耗增加.
(2)碳化反应可生成Mg(HCO3)2,生成Mg(HCO3)2的化学方程式为Mg(OH)2+2CO2═Mg(HCO3)2.
(3)流程图中煅烧反应和热解反应可以为碳化反应提供二氧化碳源.
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去.常温时当调节溶液pH为9.5时,此时Mn2+小于10-5mol/L,不会沉淀出来.
②如果把Fe2+转化为Fe3+,从环境角度选择最合适的氧化剂为C.
A.Ca(C1O)2 B.Cl2 C.H2O2 D.HNO3
③下列方案中,较好的为方案2,理由是加入碳酸钠的产品中易混入更多杂质,不易提纯.


(1)根据下列表格数据,选择消化反应的最佳温度70℃;理由是温度进一步升高同等幅度,转化率几乎不变,但能耗增加.
| 消化温度/℃ | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
| 转化率/% | 50.3 | 58.2 | 85.1 | 85.2 | 90.7 | 91.2 | 91.5 |
(3)流程图中煅烧反应和热解反应可以为碳化反应提供二氧化碳源.
(4)有工艺设计利用卤水碳化法制取轻质碳酸镁:
①卤水中含有Fe2+和Mn2+,当其浓度小于1×10-5时,可以认为完全除去.常温时当调节溶液pH为9.5时,此时Mn2+小于10-5mol/L,不会沉淀出来.
| 物质 | Mg(OH)2 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| Ksp | 10-11 | 10-39 | 10-17 | 10-14 |
A.Ca(C1O)2 B.Cl2 C.H2O2 D.HNO3
③下列方案中,较好的为方案2,理由是加入碳酸钠的产品中易混入更多杂质,不易提纯.

12.下列根据实验操作和现象得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
| B | 向甲苯中滴加少量酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
| C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
| A. | A | B. | B | C. | C | D. | D |