题目内容
16.下列离子方程式错误的是( )| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | (NH4) 2Fe (SO4) 2溶液与过量NaOH 溶液反应:Fe2++2OH-═Fe(OH)2↓ | |
| C. | 向 NaAlO2溶液中通过里 CO2:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| D. | 酸性 KMnO4 氧化 H2O2:MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O |
分析 A.氢氧化钡与稀硫酸反应生成硫酸钡沉淀和水;
B.氢氧化钠过量,铵根离子和亚铁离子都参与反应;
C.二氧化碳过量,反应生成氢氧化铝沉淀和碳酸氢钠;
D.酸性高锰酸钾溶液具有强氧化性,能够将双氧水氧化成氧气.
解答 解:A.向Ba(OH)2溶液中滴加稀硫酸,反应的离子方程式为:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O,故A正确;
B.(NH4) 2Fe (SO4) 2溶液与过量NaOH 溶液反应生成硫酸钠、一水合氨和氢氧化亚铁沉淀,正确的离子方程式为:Fe2++2NH4++4OH-═Fe(OH)2↓+2NH3•H2O,故B错误;
C.向 NaAlO2溶液中通过量CO2,反应的离子方程式为:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3-,故C正确;
D.酸性 KMnO4 氧化 H2O2,二者发生氧化还原反应,反应的离子方程式为:MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O,故D正确;
故选B.
点评 本题考查了离子方程式的书写判断,题目难度中等,注意明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
6.在稀硫酸中放入一块镀层被严重损坏的镀锌铁板(俗称白铁片),反应放出气体的速率是( )
| A. | 时快时慢 | B. | 先慢后快 | C. | 先快后慢 | D. | 保持不变 |
1.锂空气电池是一种新型的二次电池,其放电时的工作原理如图所示,下列说法正确的是( )
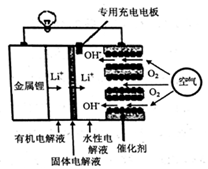

| A. | 正极区产生的LiOH可回收利用 | |
| B. | 电池中的有机电解液可以用稀盐酸代替 | |
| C. | 该电池放电时,正极的反应式为O2+4e-+4H+=2H2O | |
| D. | 该电池充电时,阴极发生了氧化反应:Li++e-=Li |
5.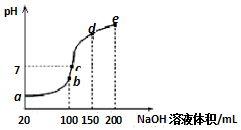 常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
 常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )
常温下,现向50mL 0.1mol•L-1 NH4HSO4溶液中滴加0.05mol•L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生).下列说法正确的是( )| A. | b点溶液中离子浓度由大到小的顺序为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 图中b、c、d、三点溶液中水的电离程度最大的是c点 | |
| C. | b点后滴加NaOH溶液过程中,NH3•H2O的电离程度逐渐减小 | |
| D. | pH=7时,溶液中c(H+)+c(Na+)+c(NH4+)=c(SO42-)+c(OH-) |

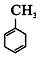 的官能团名称为碳碳双键.
的官能团名称为碳碳双键. 的系统命名为2-丙酮酸,则A的名称是3-丁酮酸.
的系统命名为2-丙酮酸,则A的名称是3-丁酮酸.
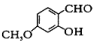 中能与稀NaOH溶液反应的官能团是羟基.检验该官能团的方法是取少量样品,加入氯化铁溶液,如果显紫色,则说明含有酚羟基.
中能与稀NaOH溶液反应的官能团是羟基.检验该官能团的方法是取少量样品,加入氯化铁溶液,如果显紫色,则说明含有酚羟基.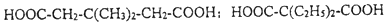 .
.
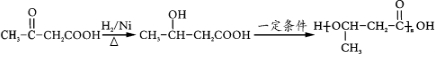 .(无机试剂任用)
.(无机试剂任用)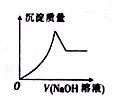 某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干种离子.某同学对该溶液进行了如下实验:
某水溶液X中只可能含有Al3+、CO32-、Cl-、SiO32-、SO42-、Fe2+中的若干种离子.某同学对该溶液进行了如下实验: