题目内容
11.基于以下实验现象,下列实验操作和结论均正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的等浓度的HCOONa溶液、CH3COONa溶液的pH | pH(HCOONa)<pH(CH3COONa) | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向0.5ml 2mol/L的NaOH溶液中加入1ml 1mol/L的CuSO4溶液,振荡后再加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.水解后显碱性,pH越大,对应酸的酸性越弱;
B.检验-CHO,应在碱性条件下;
C.KBrO3溶液中加入少量苯,然后通入少量Cl2,有机相呈橙色,说明该反应中有Br2生成,Br元素化合价由+5价变为0价,所以KBrO3是氧化剂,则Cl2是还原剂;
D.NaAlO2溶液促进的NaHCO3溶液电离.
解答 解:A.水解后显碱性,pH越大,对应酸的酸性越弱,则pH(HCOONa)<pH(CH3COONa),可知弱酸的酸性:HCOOH>CH3COOH,故A正确;
B.检验-CHO,应在碱性条件下,操作中碱不足,不能检验,故B错误;
C.KBrO3溶液中加入少量苯,然后通入少量Cl2,有机相呈橙红色,说明该反应中有Br2生成,Br元素化合价由+5价变为0价,所以KBrO3是氧化剂,则Cl2是还原剂,可知氧化性为KBrO3>KClO3,故C错误;
D.NaAlO2溶液促进的NaHCO3溶液电离,生成沉淀,与水解无关,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握盐类水解、氧化还原反应、有机物的性质为解答的关键,侧重分析与应用能力的考查,注意反应原理与实验的结合,题目难度不大.

练习册系列答案
相关题目
2.甲物质与强碱溶液反应只生成盐和水,甲一定不属于( )
| A. | 酸 | B. | 盐 | C. | 金属单质 | D. | 氧化物 |
19.下列试剂保存方法正确的是( )
| A. | 氯水保存在棕色试剂瓶中 | |
| B. | 氢氧化钠溶液保存在带有玻璃塞的玻璃试剂瓶中 | |
| C. | 金属钠保存在水中 | |
| D. | 氢氟酸保存在玻璃试剂瓶中 |
4.下列说法正确的是( )
| A. | 吸热反应只有在加热或点燃的条件下才能进行 | |
| B. | H2SO4与Ca(OH)2溶液反应的中和热△H=2×(-57.3kJ•mol-1) | |
| C. | CH4的燃烧热为-890.31kJ•mol-1,它表示1mol CH4完全燃烧生成CO2和液态水时放出890.31kJ热量 | |
| D. | 反应是放热还是吸热由反应物和生成物所具有的能量的相对大小决定 |
8.下列离子化合物中,阴阳离子间的距离最大的是( )
| A. | LiCl | B. | NaCl | C. | KCl | D. | KBr |
9.下列离子方程式正确的是( )
| A. | 氢氧化钡溶液与硫酸镁溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 向Ca(ClO)2溶液中通入少量二氧化硫:Ca2++2ClO-+H2O+SO2═2HClO+CaSO3↓ | |
| C. | 向氯化铁溶液中通入氨气:Fe3++3OH-═Fe(OH)3↓ | |
| D. | 氧化钠与冷水反应:Na2O+H2O═2Na++2OH- |
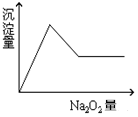 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.


