题目内容
1.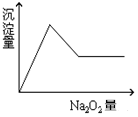 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
分析 加入Na2O2粉末,过氧化钠与水反应,2Na2O2+2H2O=4NaOH+O2↑,并同时析出白色沉淀,故可推断不含有H+、Cu2+,氨气具有刺激性气味,故不含有NH4+;当加入过量的过氧化钠时,先生成白色沉淀,后沉淀部分溶解,推断一定有Mg2+、Al3+,可能含有Na+,以此解答该题.
解答 解:加入Na2O2粉末,过氧化钠与水反应,2Na2O2+2H2O=4NaOH+O2↑,并同时析出白色沉淀,故可推断不含有H+、Cu2+,氨气具有刺激性气味,故不含有NH4+;当加入过量的过氧化钠时,先生成白色沉淀,后沉淀部分溶解,推断一定有Mg2+、Al3+,可能含有Na+,含有Mg2+、Al3+,则一定不含CO32-,由溶液的电中性可知含有Cl-,
答,溶液一定含有Mg2+、Al3+、Cl-,可能含有Na+.
点评 本题考查了离子检验方法,该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难度较大,有利于培养学生的逻辑思维能力和发散思维能力,提高学生的应试能力和学习效率.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
13.下列说法不正确的是( )
| A. | 与Na反应时,乙醇的反应速率比水慢 | |
| B. | 除去乙烷中混有的少量乙烯的方法是通入溴水 | |
| C. | 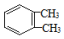 和 和 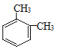 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 是同一种物质,说明苯分子中的碳碳键不是单双键交替的 | |
| D. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 |
12.下列说法正确的是( )
| A. | 记录Na2S2O3与稀硫酸的反应时间,应从溶液混合时开始计时,到刚出现浑浊结束 | |
| B. | 将少量溴乙烷与氢氧化钾水溶液充分反应,应先加硝酸酸化,然后在试管中加入AgNO3溶液,观察是否出现浅黄色沉淀,该实验可检验溴乙烷中是否含有溴元素 | |
| C. | 将两块未擦去氧化膜的铝片分别投入1mol•L-1CuSO4和1mol•L-1CuCl2溶液中,铝片表面都观察不到明显的反应现象 | |
| D. | 人体吸入氯气、氯化氢气体时,可吸入少量酒精或乙醚的混合气体解毒;氨气、溴中毒休克时要马上进行人工呼吸 |
9.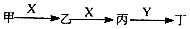 甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )
甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )
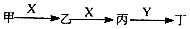 甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )
甲、乙、丙、丁四种物质中,丁为难溶于水的物质,在一定条件下,它们之间具有如图转化关系(部分反应物、生成物和反应条件未列出).下列有关物质的推断不正确的是( )| A. | 若甲为C,则Y可能是Ba(OH)2溶液 | B. | 若甲为CO2,则Y可能是FeCl3溶液 | ||
| C. | 若甲为NH3,则Y可能是NaOH | D. | 若甲为S,则Y可能是BaC12溶液 |
16.关于恒容密闭容器进行的反应C(s)+CO2(g)?2CO(g)△H>0.下列说怯不正确的是( )
| A. | △s>0 | |
| B. | 在低温下能自发进行 | |
| C. | 当混合气体的密度不再变化时.反应达到平衡 | |
| D. | 达到平衡时,升高温度,CO2的转化率和反应速率均增大 |
6.下列说法不正确的是( )
| A. | 干冰中分子的堆积方式为非密堆积 | |
| B. | 金属晶体中原子的最大配位数为12 | |
| C. | 晶体硅熔化时需破坏非极性共价键 | |
| D. | 冰融化为水的过程中其密度先变大,超过4℃后又逐渐变小 |
13.足量下列溶液与相同质量的铝反应放出氢气,消耗溶质物质的量最少的是( )
| A. | NaOH溶液 | B. | 稀硫酸 | C. | 盐酸 | D. | Ba(OH)2溶液 |
10.已知298K时,CO2(g)的△H为-393.5kJ•mol-1,H2O(l)的△H=-285.8kJ•mol-1,乙炔的燃烧热为-1300kJ•mol-1,则乙炔的标准生成热为( )
| A. | 227.2kJ•mol-1 | B. | -227.2kJ•mol-1 | C. | 798.8kJ•mol-1 | D. | -798.8kJ•mol-1 |
11.基于以下实验现象,下列实验操作和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 测定常温时的等浓度的HCOONa溶液、CH3COONa溶液的pH | pH(HCOONa)<pH(CH3COONa) | 弱酸的酸性:HCOOH>CH3COOH |
| B | 向0.5ml 2mol/L的NaOH溶液中加入1ml 1mol/L的CuSO4溶液,振荡后再加入0.5ml有机物X,加热 | 未出现砖红色沉淀 | 说明X中不含有醛基 |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2 | 有机相呈橙红色 | 氧化性:Cl2>Br2 |
| D | NaAlO2溶液与NaHCO3溶液混合 | 有白色絮状沉淀生成 | 二者水解相互促进生成氧化铝沉淀 |
| A. | A | B. | B | C. | C | D. | D |