题目内容
7.在隔绝空气的条件下发生反应:CH4(g)=C(g)+2H2(g)△H>0,下列说法正确的是( )| A. | 低温下是非自发反应,高温下是自发反应 | |
| B. | 任何温度下都是自发反应 | |
| C. | 低温下是自发反应,高温下是非自发反应 | |
| D. | 任何温度下都是非自发反应 |
分析 CH4(g)=C(g)+2H2(g)△H>0,由化学计量数可知△S>0,△H-T△S<0的反应可自发进行,以此来解答.
解答 解:CH4(g)=C(g)+2H2(g)△H>0,由化学计量数可知△S>0,则该反应在高温下△H-T△S<0,反应可自发进行,
故选A.
点评 本题考查反应热与焓变,为高频考点,把握焓变、熵变及反应进行方向的判断为解答的关键,侧重分析与应用能力的考查,注意综合判据的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.一定量的混合气体在密闭容器中发生反应:mA(g)+nB(g)?pC(g)达到平衡时,维持温度不变,将气体体积缩小到原来的$\frac{1}{2}$,当达到新的平衡时,气体C的浓度变为原平衡时的1.9倍,则下列说法正确的是( )
| A. | m+n>p | B. | m+n<p | ||
| C. | 平衡向正反应方向移动 | D. | C的质量分数增加 |
18.在下列各组溶液中,离子一定能大量共存的是( )
| A. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- | |
| B. | NaHCO3溶液中:Na+、K+、SO42-、AlO2- | |
| C. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| D. | 水电离出的c(H+)=1×10-13mol/L的溶液:Na+、K+、AlO2-、CO32- |
15.下列有关实验叙述及操作正确的是( )
| A. |  观察Fe(OH)2的生成 | |
| B. | 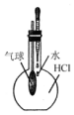 用图所示方法验证HCl气体易溶于水 | |
| C. | 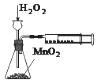 用图定量测定H2O2的分解速率 | |
| D. | 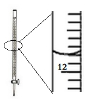 记录滴定终点读数为12.20mL |
2.下列反应既属于氧化还原反应,又属于吸热反应的是( )
| A. | Na2O2与H2O反应 | B. | 灼热的木炭与水蒸气反应 | ||
| C. | 铝热反应 | D. | CH4与O2反应 |
12.Li-SOCl2电池是迄今具有最高能量比的电池.该电池中锂为负极,碳棒为正极,无水四氯铝酸锂(LiAlCl4)的SOCl2溶液为电解液.电池总反应为电池的总反应可表示为:4Li+2SOCl2=4LiCl+SO2+S.下列说法不正确的是( )
| A. | 负极的电极反应式为 Li-e-=Li+ | |
| B. | 正极的电极反应式为2SOCl2+4e-=SO2+S+4Cl- | |
| C. | 若电解液中含有水,则该电池的效率将大大降低 | |
| D. | 若负极有14gLi参加反应,则理论上流过电路中的电子书约为1.204×1023 |
19.钢铁在海水中的锈蚀过程示意见图,有关说法正确的是( )
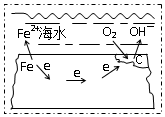

| A. | 电子从碳转移给铁 | |
| B. | 在钢铁上连接铅块,可起到防护作用 | |
| C. | 正极反应为:O2+2H2O+4e→4OH- | |
| D. | 该金属腐蚀过程为析氢腐蚀 |
10.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K、Cl-、MnO4-、SO42- | B. | Na+、SO42-、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Ca2+、SO42-、S2-、Cl- |