题目内容
7.下列说法正确的是( )| A. | 物质发生化学变化一定伴随着能量变化 | |
| B. | 升高温度或加入催化剂,可以改变化学反应的反应热 | |
| C. | 据能量守恒定律,反应物的总能量一定等于生成物的总能量 | |
| D. | 热化学方程式中,如果没有注明温度和压强,则表示反应热是在标准状况下测得的 |
分析 A.化学反应中一定伴随着物质和能量变化;
B.催化剂不影响反应热;
C.反应中存在能量变化,则反应物与生成物的总能量一定不相等;
D.在常温、常压下,焓变可以不标温度和压强.
解答 解:A.物质发生化学变化时一定存在化学键的断裂与形成,则一定伴随着能量变化,故A正确;
B.升高温度可以改变化学反应的反应热,但使用催化剂只影响反应速率,不影响反应热,故B错误;
C.据能量守恒定律,反应物的总能量=生成物的总能量+放出能量(-吸收能量),故C错误;
D.没有注明温度和压强,则表示反应热是在通常状况下测得的数据,故D错误;
故选A.
点评 本题考查了热化学方程式书写、催化剂对焓变的影响、能量守恒定律,题目难度不大,学习中注意相关基础知识的积累.

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
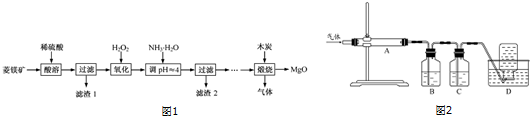
17. 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是反应条件不易控制,若控温不当易生成Cu而使Cu2O产率降低.
(2)已知:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-akJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-bkJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-ckJ•mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=-(b-2c-$\frac{a}{2}$)kJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)变化如表所示.
下列叙述正确的是C(填字母代号).
A.实验的温度:T2<T1
B.实验①前20min的平均反应速率 v(O2)=7×10-5 mol•L-1 min-1
C.实验②比实验①所用的催化剂催化效率高.
 纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:| 方法Ⅰ | 用炭粉在高温条件下还原CuO |
| 方法Ⅱ | 电解法,反应为2Cu+H2O $\frac{\underline{\;电解\;}}{\;}$ Cu2O+H2↑. |
| 方法Ⅲ | 用肼(N2H4)还原新制Cu(OH)2 |
(2)已知:2Cu(s)+$\frac{1}{2}$O2(g)=Cu2O(s)△H=-akJ•mol-1
C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-bkJ•mol-1
Cu(s)+$\frac{1}{2}$O2(g)=CuO(s)△H=-ckJ•mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)=Cu2O(s)+CO(g);△H=-(b-2c-$\frac{a}{2}$)kJ•mol-1.
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极生成Cu2O反应式为2Cu-2e-+2OH-=Cu2O+H2O.
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2.该制法的化学方程式为4Cu(OH)2+N2H4$\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2↑+6H2O.
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:2H2O(g)$?_{Cu_{2}O}^{光照}$2H2(g)+O2(g)△H>0,水蒸气的浓度(mol/L)随时间t(min)变化如表所示.
| 序号 | 温度 | 0 | 10 | 20 | 30 | 40 | 50 |
| ① | T1 | 0.050 | 0.0492 | 0.0486 | 0.0482 | 0.0480 | 0.0480 |
| ② | T1 | 0.050 | 0.0488 | 0.0484 | 0.0480 | 0.0480 | 0.0480 |
| ③ | T2 | 0.10 | 0.094 | 0.090 | 0.090 | 0.090 | 0.090 |
A.实验的温度:T2<T1
B.实验①前20min的平均反应速率 v(O2)=7×10-5 mol•L-1 min-1
C.实验②比实验①所用的催化剂催化效率高.
18.某氯原子的质量是ag,12C原子的质量是b g,用NA表示阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 该氯原子的相对原子质量为$\frac{a}{b}$ | |
| B. | m g该氯原子的物质的量为$\frac{m}{a{N}_{A}}$mol | |
| C. | 该氯原子的摩尔质量为aNAg | |
| D. | a g该氯原子所含的电子数为17 mol |
15.下列关于胶体应用与其性质的对应不正确的是( )
| A. | 鉴别胶体与浊液(丁达尔效应) | B. | 高压除尘(电泳现象) | ||
| C. | 河海交汇处可沉积沙洲(聚沉) | D. | 喷雾剂的应用(布朗运动) |
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,92 g NO2和N2O4混合气体含有的原子数为6 NA | |
| B. | 5.6 g金属铁与足量稀盐酸反应,失去的电子数为0.3 NA | |
| C. | 标准状况下,ll.2 LSO3含有的分子数为0.5 NA | |
| D. | 25℃、101 kPa时,64 g SO2中含有的氧原子数为3 NA |
12.将X、Y、Z三块金属分别用导线两两相连浸入稀H2SO4中组成原电池.X、Y相连时,X为负极;Z、Y相连时,电流由Y→Z;Z、X相连时,Z极上产生大量气泡.这三种金属的活动顺序正确的是( )
| A. | X>Z>Y | B. | Z>X>Y | C. | X>Y>Z | D. | Y>Z>X |
19.下列化学实验操作中均要用到玻璃棒,其中玻璃棒作用相同的是( )
①过滤
②蒸发
③溶解
④向容量瓶转移液体
⑤测溶液的pH值.
①过滤
②蒸发
③溶解
④向容量瓶转移液体
⑤测溶液的pH值.
| A. | ①②④ | B. | ②③⑤ | C. | ①和④ | D. | ③和④ |
16.不同温度下,水溶液中c(H+)与 c(OH+)的关系如图所示,下列说法正确的是( )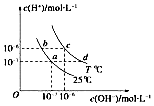

| A. | 若从a点到c点,可采用在水中加入酸的方法 | |
| B. | b点对应的醋酸中由水电离的c(H+)=10-6mol•L-1 | |
| C. | T℃时,0.05 mol•L-1的Ba(OH)2溶液的pH=11 | |
| D. | c点对应溶液的Kw大于d点对应溶液的Kw |