籾朕坪否
15⤴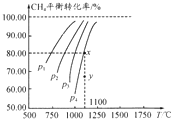 壓匯否持音延議畜液否匂嶄割秘0.1mol/LCO2才0.1mol/LCH4⇧壓匯協訳周和窟伏郡哘⦿CH4↙g⇄+CO2↙g⇄?2CO↙g⇄+2H2↙g⇄⤴霞誼峠財扮CH4議廬晒楕嚥梁業、儿膿議購狼泌夕⤴和双嗤購傍隈屎鳩議頁↙ ⇄
壓匯否持音延議畜液否匂嶄割秘0.1mol/LCO2才0.1mol/LCH4⇧壓匯協訳周和窟伏郡哘⦿CH4↙g⇄+CO2↙g⇄?2CO↙g⇄+2H2↙g⇄⤴霞誼峠財扮CH4議廬晒楕嚥梁業、儿膿議購狼泌夕⤴和双嗤購傍隈屎鳩議頁↙ ⇄| A⤴ | 貧峰郡哘議@H〽0 | |
| B⤴ | 儿膿P1﹅P2﹅P3﹅P4 | |
| C⤴ | 1100≧扮乎郡哘議峠財械方埃葎1.64 | |
| D⤴ | 儿膿葎P4扮⇧y泣議v屎〽v剃 |
蛍裂 A、昧梁業議幅互廬晒楕奐寄◉
B、奐寄儿膿⇧峠財﨑賑悶悶持受弌議圭﨑卞強◉
C、旋喘眉粁塀柴麻竃峠財扮議敵業箔麻◉
D、y泣扮遮莱議廬晒楕弌⇧峠財屎﨑卞強⤴
盾基 盾⦿A、貫夕嵆蛍裂⇧昧梁業幅互廬晒楕奐寄⇧屎郡哘簾犯⇧@H﹅0⇧絞A危列◉
B、儿膿奐寄⇧峠財﨑剃郡哘圭﨑卞強⇧遮莱議廬晒楕延弌⇧絞P4﹅P3﹅P2﹅P1⇧絞B危列◉
C、郡哘 CH4↙g⇄+CO2↙g⇄?2CO↙g⇄+2H2↙g⇄⇧
軟兵↙mol/L⇄ 0.1 0.1 0 0
延晒↙mol/L⇄ 0.08 0.08 0.16 0.16
峠財↙mol/L⇄ 0.02 0.02 0.16 0.16
峠財械方K=$\frac{0.1{6}^{2}〜0.1{6}^{2}}{0.02〜0.02}$=1.64⇧絞C屎鳩◉
D、壓y泣⇧遮莱議廬晒楕弌噐峠財扮議廬晒楕⇧峠財屎﨑卞強⇧V屎﹅V剃⇧絞D危列⤴
絞僉C⤴
泣得 云籾深臥阻峠財鞭梁業、儿膿議唹峒遇卞強議諒籾⇧廣吭心彈夕嵆頁盾籾議購囚⇧佃業嶄吉⤴

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
5⤴購噐剳晒珊圻郡哘才宣徨郡哘⇧和双傍隈屎鳩議頁↙ ⇄
〙署奉壓郡哘嶄峪嬬恬珊圻質⇧掲署奉壓郡哘嶄峪嬬恬剳晒質◉
〖剳晒質窟伏剳晒郡哘◉
〗珊圻質払肇窮徨⇧晒栽勺幅互◉
∠卑匣嶄議宣徨郡哘音辛嬬頁剳晒珊圻郡哘◉
⊥窟伏宣徨郡哘朔⇧卑匣議擬窮來受樋⤴
〙署奉壓郡哘嶄峪嬬恬珊圻質⇧掲署奉壓郡哘嶄峪嬬恬剳晒質◉
〖剳晒質窟伏剳晒郡哘◉
〗珊圻質払肇窮徨⇧晒栽勺幅互◉
∠卑匣嶄議宣徨郡哘音辛嬬頁剳晒珊圻郡哘◉
⊥窟伏宣徨郡哘朔⇧卑匣議擬窮來受樋⤴
| A⤴ | 〙〖∠ | B⤴ | 〙〗⊥ | C⤴ | 〖〗⊥ | D⤴ | 峪嗤〗 |
3⤴和双嗤購窮晒僥議夕幣⇧頼畠屎鳩議頁↙ ⇄
| A⤴ | 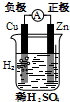 Cu-Zn圻窮学 | B⤴ | 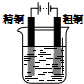 CuSO4卑匣間有議娼繕 | ||
| C⤴ |  NnCl2卑匣鑓頭尭仗 | D⤴ | 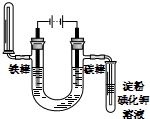 吋才NaCl卑匣刮屬賑悶恢麗 |
10⤴和双糞刮^荷恬才孖嵆 ̄嚥^潤胎 ̄脅屎鳩議頁↙ ⇄
| 荷恬才孖嵆 | 潤 胎 | |
| A | 﨑腹嗤2mL0.1mol/LAgNO3卑匣議編砿嶄⇧枠砧叱砧0.1mol/LKCl卑匣⇧壅砧紗0.1mol/LKI卑匣⤴編砿嶄枠竃孖易弼柿牛⇧朔竃孖記仔弼柿牛 | Ksp↙AgCl⇄〽Ksp↙AgI⇄ |
| B | 﨑廾嗤Fe↙NO3⇄2卑匣議編砿嶄紗秘叱砧蓮H2SO4卑匣冲弼児云音延 | Fe↙NO3⇄2嚥H2SO4音郡哘 |
| C | 壓蛍匣息況嶄紗秘汲邦朔壅紗秘CCl4⇧割蛍尅鬼⇧蛍蚊⇧和蚊卑匣格從弼 | CCl4辛恬葎汲議殕函質 |
| D | 霞協吋才NaClO卑匣、CH3COONa卑匣議pH⇧pH↙NaClO⇄﹅pH↙CH3COONa⇄ | 樋磨議磨來⦿HClO〽CH3COOH |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
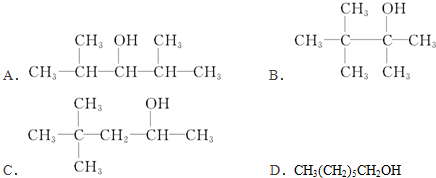
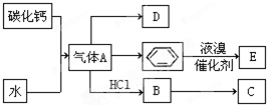
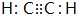 ◉D議恷酒塀CH2=CH2◉
◉D議恷酒塀CH2=CH2◉ +Br2 $\stackrel{FeBr_{3}}{★}$
+Br2 $\stackrel{FeBr_{3}}{★}$ +HBr⇧凪郡哘窃侏葎函旗郡哘⤴B★C議晒僥圭殻塀nCH2=CHCl$\stackrel{岸晒質}{★}$
+HBr⇧凪郡哘窃侏葎函旗郡哘⤴B★C議晒僥圭殻塀nCH2=CHCl$\stackrel{岸晒質}{★}$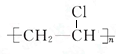 ⇧凪郡哘窃侏葎紗詔郡哘⤴
⇧凪郡哘窃侏葎紗詔郡哘⤴

 ⤴
⤴ ⤴
⤴ ⤴
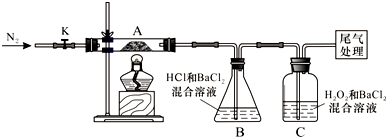
⤴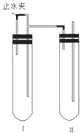 喘和中曾嶽圭隈辛參崙誼易弼議Fe↙OH⇄2柿牛⤴
喘和中曾嶽圭隈辛參崙誼易弼議Fe↙OH⇄2柿牛⤴