题目内容
7.“摩尔盐”[(NH4)2Fe(SO4)2•6H2O]是分析化学中的重要试剂.查阅文献得知:“摩尔盐”隔绝空气加热至500℃时可完全分解,但产物复杂.某学习小组欲探究其分解产物.Ⅰ.【提出猜想】摩尔盐受热分解,小组同学认为分解产物可能有以下几种情况:
a.Fe2O3、SO3、NH3、H2O b.FeO、NH3、SO3、H2O
c.FeO、SO2、NH3、H2O d.Fe2O3、NH3、SO2、SO3、H2O
经认真分析,通过推理即可确定,猜想ac不成立(填序号).
Ⅱ.【实验探究】为检验分解产物,甲同学设计了如下实验装置.
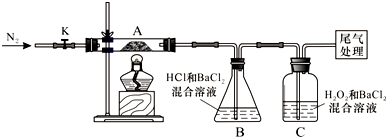
请回答下列问题:
(1)B装置的容器名称是锥形瓶.
(2)取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,目的是使分解产生的气体在B、C中被吸收充分.
(3)观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为SO2+H2O2+Ba2+=BaSO4↓+2H+.
(4)待A中剩余固体冷却至室温后,取少量置于试管中,加入稀硫酸溶解,再滴几滴KSCN溶液,可以观察到的现象是溶液变红色.
(5)乙同学设计实验验证A中残留物不含FeO,操作方法及实验现象是:取少量A中残留物放入试管中,加稀硫酸溶解,再滴加K3[Fe(CN)6]溶液,不产生蓝色沉淀,说明没有Fe2+.
Ⅲ.【实验反思】
乙同学认为:装置B中产生白色沉淀不能证明分解产物中一定含SO3,原因是分解产生的氨气消耗完B装置中的HCl后,过量的氨气存在时二氧化硫与BaCl2溶液反应生成白色沉淀.
分析 I.摩尔盐中N为-3价,Fe为+2价,S为+6价,根据产物中化合价分析,a 中生成Fe2O3,只有铁元素的化合价升高,没有元素化合价降低,c中生成FeO、SO2,其中铁元素和硫元素的化合价均降低,但是没有元素化合价升高,不符合电荷守恒;
II.取一定量“摩尔盐”置于加热管A中,加热至分解完后打开K,再通入N2,使分解产生的气体在B、C中被吸收充分,分解得到气体通过甲同学设计了的实验装置,观察到A中固体逐渐变为红棕色,说明生成物中含氧化铁,B、C中均产生白色沉淀,证明生成气体中一定含二氧化硫和三氧化硫,
(1)根据装置图分析;
(2)A中固体充分加热较长时间后,通入氮气目的是使分解生成的气体在BC装置中完全吸收;
(3)C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4;
(4)A中固体逐渐变为红棕色说明有氧化铁生成,用硫酸溶解,溶液中有Fe3+;
(5)把固体用非氧化性酸溶解,再用K3[Fe(CN)6]溶液检验,乙同学设计实验验证A中残留物不含FeO,考虑是检验二价亚铁离子,操作方法及实验现象是:取少量A中残留物放入试管中,加入稀硫酸(盐酸)溶解,再滴加K3[Fe(CN)6]溶液,不产生蓝色沉淀;
III.氨气过量时,二氧化硫与氨气生成亚硫酸铵,再与BaCl2溶液反应生成白色沉淀.
解答 解:I.摩尔盐中N为-3价,Fe为+2价,S为+6价,
a.Fe2O3、SO3、NH3、H2O 反应时只有Fe元素的化合价升高,不符合氧化还原反应规律,故a错误;
b.FeO、NH3、SO3、H2O,反应时没有元素化合价的变化,只是发生分解反应,故b正确;
c.FeO、SO2、NH3、H2O反应时只有S元素的化合价降低,不符合氧化还原反应规律,故c错误;
d.Fe2O3、NH3、SO2、SO3、H2O反应时,Fe的化合价升高,S的化合价降低,符合氧化还原反应规律,故d正确.
故答案为:ac;
II.(1)由装置图可知,B装置是锥形瓶;故答案为:锥形瓶;
(2)A中固体充分加热较长时间后,产生气体有一部分残留在装置中,通入氮气可以使分解生成的气体在B、C装置中完全吸收;
故答案为:使分解产生的气体在B、C中被吸收充分;
(3)C中有白色沉淀生成,是因为SO2被双氧水氧化成SO42-,SO42-再与Ba2+结合成沉淀BaSO4则C中发生的反应为SO2+H2O2+Ba2+=BaSO4↓+2H+;
故答案为:SO2+H2O2+Ba2+=BaSO4↓+2H+;
(4)A中固体逐渐变为红棕色说明有氧化铁生成,用硫酸溶解,溶液中有Fe3+,在溶液中滴几滴KSCN溶液,则溶液会变红色;
故答案为:溶液变红色;
(5)要验证A中残留物不含FeO,先取少量A中残留物放入试管中,再加入稀硫酸或盐酸溶解,然后滴加K3[Fe(CN)6]溶液检验,若不产生蓝色沉淀,说明没有Fe2+;
故答案为:加稀硫酸溶解,再滴加K3[Fe(CN)6]溶液,不产生蓝色沉淀,说明没有Fe2+;
III.氨气过量时,产生的氨气消耗完B装置中的HCl后二氧化硫与氨气生成亚硫酸铵,亚硫酸铵与BaCl2溶液反应生成BaSO3沉淀,所以不能说明分解产物中一定含SO3,故答案为:分解产生的氨气消耗完B装置中的HCl后,过量的氨气存在时二氧化硫与BaCl2溶液反应生成白色沉淀.
点评 本题考查了物质性质的实验探究和实验设计,题目涉及氧化还原反应、离子方程式的书写、离子检验、实验基本操作等,侧重于考查学生对基础知识的综合应用能力,题目难度中等.

 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案| A. | 取样,滴加AgNO3溶液,看是否有白色沉淀 | |
| B. | 取样,先加盐酸酸化,再加入AgNO3溶液,看是否有白色沉淀生成 | |
| C. | 取样,加少量AgNO3溶液,有白色沉淀,再加稀HCl,看白色沉淀是否消失 | |
| D. | 取样,加少量AgNO3溶液,有白色沉淀,再加稀HNO3,看白色沉淀是否消失 |
| A. | Na2SO3溶液中:c(H+)+c(HSO3-)+2c(H2SO3)═c(OH-) | |
| B. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| C. | 有些化学反应既属于复分解反应又属于氧化还原反应 | |
| D. | 常温下,将pH=3的HA和PH=11的BOH等体积混合后pH>7,可能生成了弱酸强碱盐 |
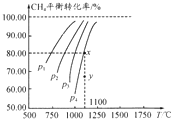 在一容积不变的密闭容器中充入0.1mol/LCO2和0.1mol/LCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g).测得平衡时CH4的转化率与温度、压强的关系如图.下列有关说法正确的是( )
在一容积不变的密闭容器中充入0.1mol/LCO2和0.1mol/LCH4,在一定条件下发生反应:CH4(g)+CO2(g)?2CO(g)+2H2(g).测得平衡时CH4的转化率与温度、压强的关系如图.下列有关说法正确的是( )| A. | 上述反应的△H<0 | |
| B. | 压强P1>P2>P3>P4 | |
| C. | 1100℃时该反应的平衡常数约为1.64 | |
| D. | 压强为P4时,y点的v正<v逆 |
| A. | 在化工生产中应遵循“绿色化学”的思想 | |
| B. | 在元素周期表的过渡元素中寻找优良的催化剂 | |
| C. | 汽车尾气中产生NO的原因是空气中的N2与O2在汽车汽缸内的高温环境下发生反应的产物 | |
| D. | 根据元素周期律,由HClO4可以类推出氟元素也存在最高价氧化物的水化物HFO4 |
| A. | C在反应中被还原 | B. | S和KNO3都发生了还原反应 | ||
| C. | CO2是反应的氧化产物 | D. | K2S和N2都是反应的还原产物 |
| A. | 充电过程是化学能转化为电能的过程 | |
| B. | 充电时阳极反应:Ni(OH)2-e-+OH-═NiOOH+H2O | |
| C. | 放电时负极附近溶液的酸性增强 | |
| D. | 放电时电解质溶液中的OH-向正极移动 |