题目内容
15.某淀粉胶体内混有盐酸和食盐,欲使胶体pH升高并除去食盐,可采用的方法是( )| A. | 盐析 | B. | 萃取 | C. | 渗析 | D. | 蒸馏 |
分析 胶粒不能透过半透膜,离子可透过,除去其中的HCl和NaCl,除去了HCl,胶体的pH当然会升高.
解答 解:在溶液中,淀粉形成胶体,淀粉胶粒大,不能透过半透膜,可用渗析法,经多次换水(或将半透膜悬挂于流动的水中),除去其中的HCl和NaCl,除去了HCl,胶体的pH当然会升高.
故选C.
点评 本题主要考查了胶体的提纯,掌握渗析的原理和各提纯方法适用对象是解答的关键,题目难度不大.

练习册系列答案
相关题目
5.下列物质中,既能跟盐酸反应,又能跟NaOH溶液反应的是( )
| A. | Na2CO3 | B. | Fe2O3 | C. | Al2O3 | D. | SiO2 |
6.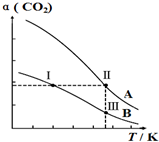 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )| A. | 反应2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g)的△S<0、△H<0 | |
| B. | 表示乙容器CO2的平衡转化率随温度变化的是曲线B | |
| C. | 体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ) | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ) |
20.下列做法中正确的是( )
| A. | 除去乙烷中少量的乙烯:与氢气混合加热,把乙烯转化为乙烷 | |
| B. | 除去苯中的少量乙烯:加入浓溴水振荡静置后过滤,除去二溴乙烯 | |
| C. | 为加快反应速率,制乙炔时用食盐水代替水 | |
| D. | 提取碘水中的碘,加入CCl4振荡静置分层后,取出有机层再分离 |
7.下列措施,能使煤炭燃烧更充分,提高热能利用率的是( )
| A. | 多加煤以使炉火更旺 | B. | 把煤炭做成大煤球 | ||
| C. | 把煤中掺合一些黄泥做成蜂窝煤 | D. | 把煤粉碎,在煤粉燃烧器中燃烧 |
8. 在元素周期表中前四周期的五种元素的位置关系如图所示.若B元素的核电荷数为Z,则五种元素的核电荷数之和为( )
在元素周期表中前四周期的五种元素的位置关系如图所示.若B元素的核电荷数为Z,则五种元素的核电荷数之和为( )
 在元素周期表中前四周期的五种元素的位置关系如图所示.若B元素的核电荷数为Z,则五种元素的核电荷数之和为( )
在元素周期表中前四周期的五种元素的位置关系如图所示.若B元素的核电荷数为Z,则五种元素的核电荷数之和为( )| A. | 5Z | B. | 5Z+18 | C. | 5Z+10 | D. | 5Z+8 |
9.偏二甲肼( )是运载火箭的主体燃料.与偏二甲肼分子式相同,分子中含碳碳单键的同分异构体共有( )
)是运载火箭的主体燃料.与偏二甲肼分子式相同,分子中含碳碳单键的同分异构体共有( )
 )是运载火箭的主体燃料.与偏二甲肼分子式相同,分子中含碳碳单键的同分异构体共有( )
)是运载火箭的主体燃料.与偏二甲肼分子式相同,分子中含碳碳单键的同分异构体共有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
 HCO3-+OH-;
HCO3-+OH-;
