题目内容
3.铁、铝、铜等金属及其化合物在日常生活中应用广泛,请回答下列问题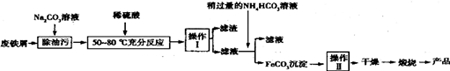
(1)生铁中含有一种铁碳化合物X(Fe3C).X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶予过量盐酸,化学方程式为Fe3O4+8HCl═2FeCl3+FeCl2+4H2O;Y与过量浓硝酸反应后溶液中含有的盐的化学式为Fe(NO3)3;
(2)某溶液中含有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是BC(填编号).
A.Mg2+ B.Fe2+ C.Al3+ D.Cu2+
(3)氧化铁是重要的工业颜料,用废铁屑制备它的流程如下:
①NaC03溶液可以除油污,原因是(用离子方程式表示)CO32-+H2O
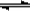 HCO3-+OH-;
HCO3-+OH-;②操作Ⅱ中沉淀的洗涤的方法是向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次;
③请写出生成FeC03沉淀的离子方程式Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
④实验室为测定产品纯度,1.040g产品中含有的Fe2O3准确值为1.015g,而实验测定结果是1.00g,测定的相对误差为±1.5%(±1.48%)(以百分比计算).
分析 (1)FeC在足量的空气中高温煅烧,生成有磁性的固体Y,Y为Fe3O4,与过量的盐酸反应生成氯化亚铁、氯化铁,溶液有剩余的HCl;硝酸具有强氧化性,Fe3O4与过量的浓硝酸反应生成硝酸铁;
(2)加入过量的NaOH,Al3+转化为偏铝酸根,Mg2+、Fe2+、Cu2+转化为氢氧化物沉淀,且氢氧化亚铁易被氧化,灼烧固体得到氧化镁、氧化铜、氧化铁,用过量的稀盐酸中,所得溶液中含有Mg2+、Fe3+、Cu2+;
(3)由制备流程可知,碳酸钠水解显碱性,可促进油污的水解,加稀硫酸除去碳酸钠,且溶解Fe,操作I为过滤,滤液中含Fe2+,与碳酸氢铵反应生成碳酸亚铁沉淀,操作II为洗涤,然后干燥、灼烧得到氧化铁,相对误差为相对值除以准确值.
解答 解:(1)FeC在足量的空气中高温煅烧,生成有磁性的固体Y,Y为Fe3O4,溶于过量的盐酸反应生成氯化亚铁、氯化铁,溶液有剩余的HCl,溶液中大量存在的阳离子是Fe2+、Fe3+、H+,硝酸具有强氧化性,Fe3O4与过量的浓硝酸反应生成硝酸铁;
故答案为:Fe3O4+8HCl═2FeCl3+FeCl2+4H2O;
(2)加入过量的NaOH,Al3+转化为偏铝酸根,Mg2+、Fe2+、Cu2+转化为氢氧化物沉淀,且氢氧化亚铁易被氧化,灼烧固体得到氧化镁、氧化铜、氧化铁,用过量的稀盐酸中,所得溶液中含有Mg2+、Fe3+、Cu2+,与原溶液相比,溶液中大量减少的阳离子是Al3+、Fe2+,
故选BC;
(3)①Na2CO3溶液可以除油污,油污在碱性条件下生成可溶解的钠盐和醇,原因是碳酸钠溶液水解呈碱性,故答案为:CO32-+H2O?HCO3-+OH-;
②由上述分析可知,操作II为洗涤,操作Ⅱ的方法为在漏斗中加入适量蒸馏水,浸没沉淀,让蒸馏水自然流下,重复2~3次,
故答案为:向漏斗中加入蒸馏水至没过固体,让水自然流出,重复2~3次;
③生成FeCO3沉淀的离子方程式为Fe2++2HCO3-═FeCO3↓+CO2↑+H2O,故答案为:Fe2++2HCO3-═FeCO3↓+CO2↑+H2O;
④相对误差为(1.000-1.015)÷1.015═-1.48%,(1.015-1.000)÷1.015=+1.48%,
故答案为:±1.5%(±1.48% ).
点评 本题考查元素化合物性质、化学工艺流程、基本操作与方案设计、盐类水解、常用化学用语等,物质的制备实验及混合物分离提纯方法选择,为高频考点,注意把握流程中发生的反应、混合物分离方法等,侧重分析与应用能力的考查,难度中的,是对所学知识的综合利用.

| A. | K+、Na+、HCO3-、SO42- | B. | K+、Cu2+、Cl-、NO3- | ||
| C. | NH4+、Al3+、Br-、SO42- | D. | Na+、Ba2+、Cl-、NO3- |
| A. | 向Na2S03溶液中加入硝酸酸化的BaCl2,有白色沉淀出现,说明Na2S03溶液已经变质 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 等体积、pH都为3的酸HCl和CH3COOH分别与足量的锌反应,放出的氢气一样多 | |
| D. | 硫酸铁可用于净水,因为三价铁离子可水解生成Fe(OH)3沉淀 |
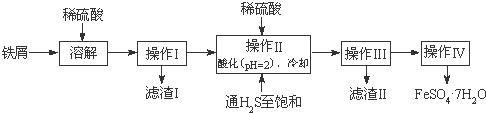
查询资料,得25℃时有关物质的数据如下表:
| 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 | |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:
①除去晶体表面附着的硫酸等杂质;
②降低洗涤过程中FeSO4•7H2O的损耗.
(3)工业上常用氧化还原滴定法测定绿矾产品中Fe2+含量,测定步骤如下:
a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol•L-1KMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①已知酸性KMnO4被FeSO4还原时生成Mn2+.写出该测定过程的离子反应方程式:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
②判断此滴定实验达到终点的方法是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
③若实验操作无失误,测得上述样品中FeSO4•7H2O的含量仍偏低,则可能的原因是部分Fe2+被空气中O2氧化;
④该绿矶产品中绿矾的质量分数为97.54%.
| A. | 盐析 | B. | 萃取 | C. | 渗析 | D. | 蒸馏 |
| A. | 稀盐酸与氢氧化钠反应 | B. | 灼热的碳与二氧化碳反应 | ||
| C. | 煅烧石灰石制生石灰 | D. | 氢氧化钡晶体与氯化铵晶体混合 |
①CH4(g)+4N02(g)═4NO(g)+C02(g)+2H20(g)△H=-574 kJ.mol-1
②CH4(g)+4NO(g)═2N2(g)+C02(g)+2H2O(g)△H=-1160kJ.mol-1
则下列选项中正确的是( )
| A. | CH4(g)+2N02(g)═N2(g)+C02(g)+2H2O(l)△H=-867 kJ.mol-1 | |
| B. | CH4催化还原1molNOx为N2的过程中,若x=1.5,则转移的电子总数为3×6.02×1021 | |
| C. | 若0.2 mol CH4还原N02至N2,在上述条件下吸收眵热迸为173.4 kJ | |
| D. | 若用4.48 LCH4还原N02至N2,整个过程中转移电子总数为1.6×6.02×1021 |