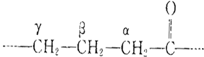题目内容
11.下列措施可以减缓盐酸与大理石反应速率的是( )| A. | 升温 | B. | 改用粉末状大理石 | ||
| C. | 加入一定量水 | D. | 加入适量浓盐酸 |
分析 为固体和溶液的反应,减小反应速率,可降低温度、减小浓度或减小固体表面积,以此解答该题.
解答 解:A.升高温度,反应速率增大,故A不选;
B.改用粉末状大理石,固体表面积增大,反应速率增大,故B不选;
C.加入一定量水,浓度减小,则反应速率减小,故C选;
D.加入适量浓盐酸,浓度增大,则反应速率增大,故D不选.
故选C.
点评 本题考查化学反应速率的影响,为高频考点,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | 燃料电池的电极包含活性物质,参与电极反应 | |
| B. | 氢氧燃料电池工作时发出蓝色火焰 | |
| C. | 铁在干燥的空气中不易生锈,在潮湿的空气中易生锈,主要是因发生电化腐蚀 | |
| D. | 温度一定时,催化剂不仅可以加快化学反应速率,而且可以改变反应物的转化率 |
2.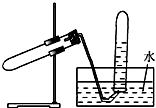 如图所示装置可用于( )
如图所示装置可用于( )
 如图所示装置可用于( )
如图所示装置可用于( )| A. | 加热NaHCO3制CO2 | B. | 用Cu和浓HNO3反应制NO2 | ||
| C. | 用Zn与稀硫酸反应制H2 | D. | 用NaCl与浓H2SO4加热制HCl |
6.如图为铜锌原电池示意图,按该装置进行实验.下列说法正确的是( )
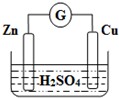

| A. | Zn是负极,Cu是正极 | B. | 稀硫酸溶液中H+移向Zn极 | ||
| C. | 电子由铜片通过导线流向锌片 | D. | 该装置能将电能转变为化学能 |
16.短周期元素X、Y、W、Q在元素周期表中位置如图所示.下列说法正确的是( )
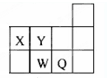

| A. | 元素X与元素Y可形成多种化合物 | |
| B. | 原子半径的大小顺序为:X>Y>W>Q | |
| C. | 还原性:W2-<Q- | |
| D. | 元素W的最高价氧化物对应水化物的酸性比Q的强 |
3.在l℃时,10mL0.4mol•L-1H2O2溶液发生催化分解:2H2O2 $\frac{\underline{\;催化剂\;}}{\;}$ 2H2O+O2↑,不同时刻测得生成O2的体积(已折算为标准状况)如下表:
下列叙述不正确的是(溶液体积变化忽略不计)( )
| t/min | 0 | 2 | 4 | 6 |
| V( 02 )/mL | 0.0 | 9.9 | 17.2 | 22.4 |
| A. | 0-2min的平均反应速率比4-6min快 | |
| B. | 0-6min 的平均反应速率v( H2O2)=3.3 x 10-2 moL-1•min-1 | |
| C. | 反应至 6min 时,c( H2O2)=0.3mol•L-1 | |
| D. | 反应至6min时,H2O2分解了 50% |
20.几种短周期元素的原子半径及主要化合价见下表:
下列叙述不正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | M的原子半径比Q的大 | |
| B. | L、T形成的简单离子核外电子数相等 | |
| C. | R、L、M三种元素的金属性依次增强 | |
| D. | Q、T两元素的氢化物的稳定性为H nT>H nQ |
13.二甲醚(CH3OCH3)是一种新型能源,利用二氧化碳合成新能源已成为环保化学家研究的热门课题.
(1)几种共价键的键能如表所示:
2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=-92KJ•mol-1.
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料.科研人员模拟光合作用,设计如图甲所示装置制备二甲醚.能量转化形式为太阳能→电能→化学能、
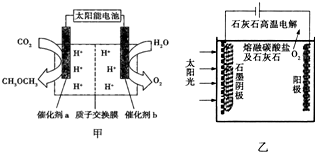
①催化剂b的电极名称是阳极.
②若释放11.2L氧气(标准状况下),有2mol H+由b移向a(填质子的迁移方向).催化剂a上的电极反应式为2CO2+12H++12e-=CH3OCH3+3H2O.
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
①生产过程中能量的转化形式是太阳能和电能转化为化学能.
②电解反应在温度小于900℃时进行,盐酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑,阴极的电极反应式为3CO2+4e-=C+2CO32-.
(1)几种共价键的键能如表所示:
| 化学键 | C═O | H-H | C-H | C-O | H-O |
| 键能/kJ•mol-1 | 803 | 436 | 414 | 326 | 464 |
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料.科研人员模拟光合作用,设计如图甲所示装置制备二甲醚.能量转化形式为太阳能→电能→化学能、

①催化剂b的电极名称是阳极.
②若释放11.2L氧气(标准状况下),有2mol H+由b移向a(填质子的迁移方向).催化剂a上的电极反应式为2CO2+12H++12e-=CH3OCH3+3H2O.
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
①生产过程中能量的转化形式是太阳能和电能转化为化学能.
②电解反应在温度小于900℃时进行,盐酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑,阴极的电极反应式为3CO2+4e-=C+2CO32-.