题目内容
13.二甲醚(CH3OCH3)是一种新型能源,利用二氧化碳合成新能源已成为环保化学家研究的热门课题.(1)几种共价键的键能如表所示:
| 化学键 | C═O | H-H | C-H | C-O | H-O |
| 键能/kJ•mol-1 | 803 | 436 | 414 | 326 | 464 |
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料.科研人员模拟光合作用,设计如图甲所示装置制备二甲醚.能量转化形式为太阳能→电能→化学能、
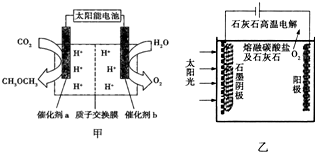
①催化剂b的电极名称是阳极.
②若释放11.2L氧气(标准状况下),有2mol H+由b移向a(填质子的迁移方向).催化剂a上的电极反应式为2CO2+12H++12e-=CH3OCH3+3H2O.
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
①生产过程中能量的转化形式是太阳能和电能转化为化学能.
②电解反应在温度小于900℃时进行,盐酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为2CO32--4e-=2CO2↑+O2↑,阴极的电极反应式为3CO2+4e-=C+2CO32-.
分析 (1)反应热等于反应物的总键能减去生成物的总键能;
(2)①催化剂b水中的氧由-2价变0价,发生氧化反应;
②电极反应式为:2H2O-4e-=4H++O2↑,若释放11.2L氧气的物质的量为0.5mol,所以有0.5mol的H+,由b移向a,a是电解池的阴极,发生还原反应,电极反应式为:2CO2+12H++12e-=CH3OCH3+3H2O;
(3)①生产过程中能量的转化形式是太阳能和电能转化为化学能;
②阳极是碳酸根离子发生氧化反应,其电极反应式为2CO32--4e-=2CO2↑+O2↑;阴极发生还原反应,其电极反应式为3CO2+4e-=C+2CO32-.
解答 解:(1)2CO2(g)+6H2(g)═CH3OCH3(g)+3H2O(g)△H=4×803+6×436-6×414-2×326-6×464=-92KJ•mol-1,故答案为:-92KJ•mol-1;
(2)①催化剂b水中的氧由-2价变0价,发生氧化反应,是电解池的阳极,故答案为:阳极;
②电极反应式为:2H2O-4e-=4H++O2↑,若释放11.2L氧气的物质的量为0.5mol,所以有0.5mol×4=2mol的H+,由b移向a,a是电解池的阴极,发生还原反应,电极反应式为:2CO2+12H++12e-=CH3OCH3+3H2O,故答案为:2;由b移向a;2CO2+12H++12e-=CH3OCH3+3H2O;
(3)①生产过程中能量的转化形式是太阳能和电能转化为化学能,故答案为:太阳能和电能转化为化学能;
②阳极是碳酸根离子发生氧化反应,其电极反应式为2CO32--4e-=2CO2↑+O2↑;阴极发生还原反应,其电极反应式为3CO2+4e-=C+2CO32-,故答案为:2CO32--4e-=2CO2↑+O2↑;3CO2+4e-=C+2CO32-.
点评 本题考查反应热的计算和电化学的相关知识,电池原理以及电极方程式的书写方法,反应热等于反应物的总键能减去生成物的总键能,题目难度不大.

 优等生题库系列答案
优等生题库系列答案| A. | 升温 | B. | 改用粉末状大理石 | ||
| C. | 加入一定量水 | D. | 加入适量浓盐酸 |
| A. | 共价键一定存在于共价化合物中,也可能存在于离子化合物中 | |
| B. | Na2O2中既含有离子键也含有极性共价键 | |
| C. | NH4Cl是都由非金属元素组成的既含有离子键也含有共价键的离子化合物 | |
| D. | 熔化状态下不导电的化合物一定是共价化合物 |
| A. | B2A3 | B. | B3A2 | C. | A2B3 | D. | BA2 |
| A. | 晶体硅具有半导体的性质,所以可以制作光导纤维 | |
| B. | 氯化铁溶液可用于制作印刷电路板是因为其具有氧化性,与铜发生置换反应 | |
| C. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| D. | 水泥厂和冶金厂常用高压直流电除去大量烟尘,减少对空气的污染 |
(1)氢氧化铝 (2)三氧化二铝 (3)铝 (4)碳酸氢钠 (5)氢氧化镁.
| A. | (1)(2)(3)(4) | B. | (1)(2)(3)(4)(5) | C. | (1)(2)(4) | D. | (1)(2)(4)(5) |
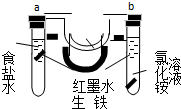 如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间.下列有关描述错误的是( )
如图装置中,U型管内为红墨水,a、b试管中分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间.下列有关描述错误的是( )| A. | a中发生了吸氧腐蚀,b中发生了析氢腐蚀 | |
| B. | 两试管中负极反应均是:Fe-2e-=Fe2+ | |
| C. | 生铁块中碳作原电池正极 | |
| D. | 红墨水在一段时间后,两边液面变为左低右高 |
 酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15g/100mL.莫尔法是较简单的一种测量Cl-含量的方法.现采用该法测量某市售酱油是否符合NaCl含量标准要求.实验原理如下(25℃):Ag++Cl-=AgCl (白色)Ksp(AgCl)=1.8×l0-10
酱油是一种常用调味剂,根据国标要求酱油中NaCl的含量不应低于15g/100mL.莫尔法是较简单的一种测量Cl-含量的方法.现采用该法测量某市售酱油是否符合NaCl含量标准要求.实验原理如下(25℃):Ag++Cl-=AgCl (白色)Ksp(AgCl)=1.8×l0-10