题目内容
3.下列关于物质或离子检验的叙述正确的是( )| A. | 在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ | |
| B. | 气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 | |
| C. | 灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+ | |
| D. | 可以用澄清石灰水,鉴别Na2CO3溶液和NaHCO3溶液 |
分析 A.如果该溶液既含Fe3+,又含Fe2+,滴加KSCN溶液,溶液呈红色,证明存在Fe3+,并不能证明无Fe2+;
B.无水硫酸铜吸水变为CuSO4•5H2O,白色粉末变蓝,可证明原气体中含有水蒸气;
C.灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,不能证明无K+,因为黄光可遮住紫光,K+焰色反应需透过蓝色的钴玻璃滤去黄光后观察;
D.二者都与石灰水反应生成沉淀.
解答 解:A.Fe3+遇KSCN会使溶液呈现红色,Fe2+遇KSCN不反应无现象,如果该溶液既含Fe3+,又含Fe2+,滴加KSCN 溶液,溶液呈红色,则证明存在Fe3+,并不能证明无Fe2+,故A错误;
B.气体通过无水硫酸铜,粉末变蓝,则发生反应:CuSO4+5H2O═CuSO4•5H2O,可证明原气体中含有水蒸气,故B正确;
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,并不能证明无K+,Na+焰色反应为黄色,可遮住紫光,K+焰色反应需透过蓝色的钴玻璃滤去黄光后观察,故C错误;
D.二者都与石灰水反应生成沉淀,不能鉴别,可加入氯化钙鉴别,故D错误.
故选B.
点评 本题考查常见物质及离子检验,题目难度中等,明确常见物质的性质及检验方法为解答关键,试题侧重对基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
9.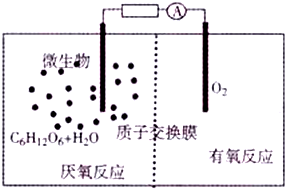 微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
 微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )
微生物电池是指在微生物的作用下将化学能转化为电能的装置(总反应方程式为C6H12O6+6O2═6CO2+6H2O),其工作原理如图所示.下列有关微生物电池的说法错误的是( )| A. | 正极区溶液的pH减小 | |
| B. | 微生物促进了反应中电子的转移 | |
| C. | 质子通过交换膜从负极区移向正极区6H2O+C6H12O6-24e-═6CO2+24H+ |
7.下列关于溶液中离子的说法正确的是( )
| A. | 0.2mol•L-1的Na2CO3溶液中离子浓度关系:c (Na+)=2c (CO32-)+c (HCO3-)+c (H2CO3) | |
| B. | 0.01mol•L-1的NH4Cl和0.01mol•L-1的NH3•H2O等体积混合后,若测得溶液中c (Cl-)>c (NH4+),则溶液中有关微粒的浓度关系: c (Cl-)>c (NH3•H2O)>c (NH4+)>c (H+)>c (OH-) | |
| C. | 0.1mol的NaHS和0.1mol的NaHSO4混合溶于水,配制成1L溶液,则混合溶液中离子浓度关系为:c (Na+)-0.1mol•L-1=2c (S2-)+c (H2S)+c (HS-) | |
| D. | 0.1mol•L-1的NaHCO3溶液中离子浓度关系:c (OH-)=c (H+)+c (H2CO3)-c (CO32-) |
15.5种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:
①C,E溶液显碱性,A,B,D溶液呈酸性,0.1mol/L的E溶液PH<13;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④将38.4g Cu片投入装有足量D溶液的试管中,Cu不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断C、D的化学式为:CBa(OH)2;DAl(NO3)3.
(2)写出步骤②中发生反应的离子反应方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)步骤④中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(4)不能确定的溶液为B和A(填字母编号).
| 阳离子 | Na+、Al 3+、Fe3+、Cu2+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO4- |
①C,E溶液显碱性,A,B,D溶液呈酸性,0.1mol/L的E溶液PH<13;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④将38.4g Cu片投入装有足量D溶液的试管中,Cu不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断C、D的化学式为:CBa(OH)2;DAl(NO3)3.
(2)写出步骤②中发生反应的离子反应方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)步骤④中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(4)不能确定的溶液为B和A(填字母编号).
12.检验溶液中的离子或物质,所用方法正确的是( )
| A. | 加入硝酸银溶液,有白色沉淀生成,证明一定有Cl-存在 | |
| B. | 加入BaCl2溶液和稀硝酸,有白色沉淀生成,证明一定有SO42- | |
| C. | 加入碳酸钠溶液产生白色沉淀,再加入盐酸白色沉淀消失,一定有Ba2+ | |
| D. | 加入氢氧化钠溶液并加热,产生的气体能使湿润的红色石蕊试纸变蓝,一定有NH4+ |
13.若NA代表阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1 mol HClO溶于水电离出NA个H+ | |
| B. | 标准状况下,11.2L的CCl4中含有0.5 NA个分子 | |
| C. | 足量Fe与1 mol Cl2充分反应,转移电子数为2NA | |
| D. | 18.0 g重水(D2O)中所含的电子数为10 NA |