题目内容
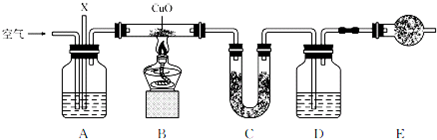
已知某气态化石燃料X中只含有碳、氢两种元素,为探究该气体中碳和氢两种元素的质量比,某同学设计了燃烧法测量的实验方案,通过测量装置C和D的增重即可求得碳和氢两种元素的质量比.实验装置如下图所示(已知CuO 可以作为碳氢化合物燃烧的催化剂):
(1)若A装置中所盛放的药品是浓NaOH 溶液,装置A的作用有:
① ;② .
(2)C装置中所盛放的药品是 ,作用是 .
(3)D装置中所盛放的药品是 ,作用是 .
(4)E装置中所盛放的药品是 ,作用是
(5)上述装置中有一处错误,请按要求填写下表(不考虑酒精灯和加热方法可能存在的错误;若增加仪器和药品,请指明仪器、药品名称和位置):
(6)若实验装置经过改正后,得到的实验数据如下:
则该气体中碳和氢两种元素的质量比为 .
(7)能否确定该燃料的分子式 ,其分子式为 .
(1)若A装置中所盛放的药品是浓NaOH 溶液,装置A的作用有:
①
(2)C装置中所盛放的药品是
(3)D装置中所盛放的药品是
(4)E装置中所盛放的药品是
(5)上述装置中有一处错误,请按要求填写下表(不考虑酒精灯和加热方法可能存在的错误;若增加仪器和药品,请指明仪器、药品名称和位置):
| 错误原因 | |
| 改正方法 | |
| 对实验结果的影响 |
| 质量 | 实验前 | 实验后 |
| 药品+U形管的质量/g | 101.1 | 102.9 |
| 药品+广口瓶D的质量/g | 312.0 | 314.2 |
(7)能否确定该燃料的分子式

考点:探究物质的组成或测量物质的含量
专题:
分析:(1)由于空气中含有CO2,会干扰燃烧产物CO2的吸收,所以必须利用氢氧化钠除去空气中的CO2.其次还可以利用A中气泡的产生的快慢来可知通入通入速率,以保证O2过量;
(2)根据燃烧产物水和CO2可知,首先应该先吸收水,然后再吸收CO2,由于C是吸收水蒸气的,而C是U型管,所以盛放的试剂是无水CaCl2或P2O5 ;
(3)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液;
(4)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
(5)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管;
(6)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,计算得到碳和氢元素的质量之比;
(7)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,n(C):n(H)=0.05:0.2=1:4,最简式为CH4,依据碳原子形成化学键特征分析判断.
(2)根据燃烧产物水和CO2可知,首先应该先吸收水,然后再吸收CO2,由于C是吸收水蒸气的,而C是U型管,所以盛放的试剂是无水CaCl2或P2O5 ;
(3)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液;
(4)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
(5)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管;
(6)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,计算得到碳和氢元素的质量之比;
(7)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,n(C):n(H)=0.05:0.2=1:4,最简式为CH4,依据碳原子形成化学键特征分析判断.
解答:
解:(1)由于空气中含有CO2,会干扰燃烧产物CO2的吸收,所以必须利用氢氧化钠除去空气中的CO2.其次还可以利用A中气泡的产生的快慢来可知通入通入速率,以保证O2过量;
故答案为:除去空气中的CO2气体; 调节X和空气的通入速率,保证O2过量;
(2)根据燃烧产物水和CO2可知,首先应该先吸收水,然后再吸收CO2.由于C是吸收水蒸气的,而C是U型管,所以盛放的试剂是无水CaCl2或P2O5;
故答案为:无水CaCl2或P2O5;吸收混合气体中的水蒸气;
(3)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液;
故答案为:浓NaOH溶液;吸收燃烧生成的二氧化碳气体;
(4)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
故答案为:碱石灰或固体NaOH;防止空气中的二氧化碳和水蒸气进入装置D,对结果产生影响;
(5)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管,加热前没有除去对本实验有影响的水蒸气,在A、B 之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管,对实验结果的影响是CH两种元素的质量比偏小;
故答案为:
(6)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,其中碳和氢元素的质量之比=0.05×12:0.1×2×1=3:1;
故答案为:3:1;
(7)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,n(C):n(H)=0.05:0.2=1:4,最简式为CH4,碳原子已饱和为甲烷的分子式CH4;
故答案为:能;CH4.
故答案为:除去空气中的CO2气体; 调节X和空气的通入速率,保证O2过量;
(2)根据燃烧产物水和CO2可知,首先应该先吸收水,然后再吸收CO2.由于C是吸收水蒸气的,而C是U型管,所以盛放的试剂是无水CaCl2或P2O5;
故答案为:无水CaCl2或P2O5;吸收混合气体中的水蒸气;
(3)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液;
故答案为:浓NaOH溶液;吸收燃烧生成的二氧化碳气体;
(4)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
故答案为:碱石灰或固体NaOH;防止空气中的二氧化碳和水蒸气进入装置D,对结果产生影响;
(5)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管,加热前没有除去对本实验有影响的水蒸气,在A、B 之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管,对实验结果的影响是CH两种元素的质量比偏小;
故答案为:
| 错误原因 | 加热前没有除去度本实验有影响的水蒸气 |
| 改正方法 | 在A、B 之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管 |
| 对实验结果的影响 | 对实验结果的影响是CH两种元素的质量比偏小 |
故答案为:3:1;
(7)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,n(C):n(H)=0.05:0.2=1:4,最简式为CH4,碳原子已饱和为甲烷的分子式CH4;
故答案为:能;CH4.
点评:本题考查有机物分子式及结构简式的判断,实验过程中装置和试剂的选择和作用分析判断,有机物的组成计算分析应用,掌握实验基础和燃烧实验的定量计算测定方法是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
235 92 |
238 92 |
235 92 |
238 92 |
238 92 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列关于某温度下一定浓度氨水的说法正确的是( )
| A、NH3?H2O电离达到平衡的标志是溶液呈电中性 | ||
B、
| ||
| C、氨水促进了水的电离 | ||
D、c(NH
|
下列物质中酸性最强的是( )
| A、HClO4 |
| B、H2SO4 |
| C、H3PO4 |
| D、H2SiO4 |
我国科学家制得了SiO2超分子纳米管,微观结构如图.下列叙述正确的是( )


| A、SiO2与干冰的晶体结构相似 |
| B、SiO2耐腐蚀,不与任何酸反应 |
| C、工业上用SiO2制备粗硅 |
| D、光纤主要成分是SiO2,具有导电性 |
 CO2和CH4都是要削减的温室气体.
CO2和CH4都是要削减的温室气体.

 b.在稀硫酸中水解有乙酸生成
b.在稀硫酸中水解有乙酸生成