题目内容
18.北京奥运会祥云火炬的外壳材料是高强度的铝镁合金.某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:方案一:铝镁合金$\stackrel{NaOH溶液}{→}$测定生成气体的体积
方案二:铝镁合金$\stackrel{盐酸}{→}$测定生成气体的体积
方案三:铝镁合金$\stackrel{盐酸}{→}$溶液$\stackrel{过量NaOH溶液}{→}$$\stackrel{过滤、洗涤、烧灼、冷却}{→}$称量灼烧产物的质量.
(1)写出方案一中发生反应的离子方程式2Al+2OH-+2H2O=2AlO2-+3H2↑.
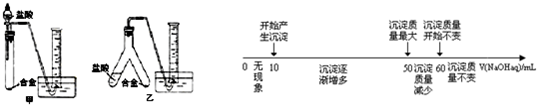
(2)实验小组根据方案二设计了两个实验装置,如图(图中的铁架台已省略).你认为选择乙(选填甲或乙)装置进行实验更合理,误差更小.
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是合金样品的质量.
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量NaOH溶液时,生成沉淀的质量与加入NaOH溶液体积的关系可用数轴关系表示.
请你判断,根据图数轴申的数据能否求出合金中镁的质量分数?能(选填“能”或“不能”).
下列①②两题选一题作答.
①若不能求出合金中镁的质量分数,请说明理由.
②若能求出合金中镁的质量分数,则镁的质量分数为30.8%(保留一位小数).
分析 (1)铝和NaOH溶液反应生成偏铝酸钠和氢气;
(2)乙装置中可以能使盐酸与合金的反应随时停止,操作简单;
(3)还需要称量合金样品的质量;
(4)加入NaOH溶液50mL~60mL为Al(OH)3与NaOH的反应,可计算Al3+的物质的量,则加入NaOH溶液10mL~50mL为Al3+和Mg2+消耗的体积,根据方程式Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓可知Al和Mg的物质的量之比,进而可计算镁的质量分数.
解答 解:(1)镁和氢氧化钠溶液不反应,但铝是可以的,反应的离子方程式是2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)根据装置构造特点可知,乙装置中可以能使盐酸与合金的反应随时停止,操作简单,所以实验更合理,误差更小,
故答案为:乙;
(3)灼烧得到的是氧化镁,所以要计算合金中镁的质量分数,还需要称量合金样品的质量,
故答案为:合金样品的质量;
(4)根据数轴可知,溶解氢氧化铝消耗的氢氧化钠溶液是60ml-50ml=10ml,则生成氢氧化铝消耗的氢氧化钠溶液体积应该是30ml,所以生成氢氧化镁消耗的氢氧化钠溶液体积是50ml-10ml-30ml=10ml,则根据方程式Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓可知Al和Mg的物质的量之比是2:1的,则镁的质量分数是$\frac{24}{24+2×27}$×100×%=30.8%,
故答案为:能;30.8%.
点评 本题考查镁铝合金中镁质量分数测定探究实验的有关判断,属于中等难度的试题,试题综合性强,在注重对基础知识巩固和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生规范严谨的实验设计能力以及评价能力,要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论.

 阅读快车系列答案
阅读快车系列答案| A. | 乙烯通入溴水中 | |
| B. | 乙烯通入酸性高锰酸钾溶液中 | |
| C. | 在水浴加热的条件下,苯与浓硝酸和浓硫酸混合液的反应 | |
| D. | 在镍做催化剂的条件下,苯与氢气反应 |
| A. | 单质钠与水的反应:Na+H2O═Na++OH-+H2↑ | |
| B. | 醋酸除水垢:2H++CaCO3═Ca2++H2O+CO2↑ | |
| C. | 氢氧化钡溶液和硫酸铜溶液反应:Ba2++SO42-═BaSO4↓ | |
| D. | 稀硫酸与铁粉反应:Fe+2H+═Fe2++H2↑ |
| A. |  定容 | B. |  收集氨气 | ||
| C. |  高温煅烧石灰石 | D. |  除去氯气中的氯化氢 |
| A. | 紫色 | B. | 红色 | C. | 蓝色 | D. | 无色 |
 .
.