题目内容
选择下列物质填空(填写序号):①金刚石 ②干冰 ③氩晶体 ④白磷 ⑤氯化钙 ⑥过氧化钠 ⑦石英 ⑧石墨 ⑨氯化铵 ⑩铜晶体
(1)固态时能导电的有 ;
(2)熔化时不破坏化学键的有 ;
(3)含有配位键的有 ;
(4)含有非极性共价键的有 .
(1)固态时能导电的有
(2)熔化时不破坏化学键的有
(3)含有配位键的有
(4)含有非极性共价键的有
考点:化学键,配合物的成键情况,极性键和非极性键
专题:化学键与晶体结构
分析:(1)含自由电子和自由离子可导电,固体导电为金属单质或石墨;
(2)熔化时不破坏化学键,应为分子构成的晶体;
(3)有空规定的原子和提供孤对电子的原子可形成配位键;
(4)同种非金属元素之间形成非极性共价键.
(2)熔化时不破坏化学键,应为分子构成的晶体;
(3)有空规定的原子和提供孤对电子的原子可形成配位键;
(4)同种非金属元素之间形成非极性共价键.
解答:
解:(1)含自由电子和自由离子可导电,固体导电为金属单质或石墨,只有⑧⑩符合,故答案为:⑧⑩;
(2)熔化时不破坏化学键,应为分子构成的晶体,只有②③④符合,故答案为:②③④;
(3)有空规定的原子和提供孤对电子的原子可形成配位键,只有⑨符合,故答案为:⑨;
(4)同种非金属元素之间形成非极性共价键,则只有①④⑥⑧符合,故答案为:①④⑥⑧.
(2)熔化时不破坏化学键,应为分子构成的晶体,只有②③④符合,故答案为:②③④;
(3)有空规定的原子和提供孤对电子的原子可形成配位键,只有⑨符合,故答案为:⑨;
(4)同种非金属元素之间形成非极性共价键,则只有①④⑥⑧符合,故答案为:①④⑥⑧.
点评:本题考查化学键,为高频考点,把握化学键形成的一般规律及化学键的判断为解答的关键,侧重基础知识的考查,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
氢离子浓度相同的等体积的盐酸A和醋酸B,分别和锌反应,若最后仅有一种溶液中存在锌,且放出氢气的质量相同,则下列说法正确的是( )
①反应所需要的时间 B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量 A=B
④反应过程的平均速率B>A
⑤盐酸里有锌剩余
⑥醋酸里有锌剩余.
①反应所需要的时间 B>A
②开始反应时的速率A>B
③参加反应的锌的物质的量 A=B
④反应过程的平均速率B>A
⑤盐酸里有锌剩余
⑥醋酸里有锌剩余.
| A、③④⑥ | B、②③⑥ |
| C、③④⑤ | D、①②⑤ |
某同学按如图所示的装置进行电解实验.下列说法不正确的是( )
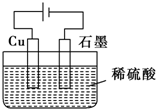

| A、电解过程中,铜电极上有H2产生 | ||||
B、电解初期,总反应方程式为 Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,H+的浓度不断减小 |
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、通常状况下,1NA个H2分子占有的体积是22.4L |
| B、1mol氧是32g |
| C、摩尔是国际七个基本物理量之一 |
| D、常温常压下,2.12gNa2CO3固体中含有的CO32-离子数位0.02NA |
下列说法正确的是( )
| A、在我们常用的元素周期表中,元素被划分为两类:金属元素和非金属元素 |
| B、在元素周期表中,每个纵列的价电子层的电子总数一定相等 |
| C、在元素周期表里,主族元素所在的族序数等于原子核外电子数 |
| D、在元素周期表中,s区,d区和ds区的元素都是金属元素 |
在一定体积的密闭容器中,进行如下的化学反应CO2(g)+H2(g)?CO(g)+H2O(g),其中
=K,K被称为化学平衡常数,其中K和温度的关系如下表:根据以上信息推断以下说法正确的是( )
| [CO]×[H20] |
| [CO2]×[H2] |
| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
| A、此反应为放热反应 |
| B、此反应只有达到平衡时,密闭容器中的压强才不会变化 |
| C、此反应达到1000℃时的反应速率比700℃时大 |
| D、该反应的化学平衡常数越大,反应物的转化率越低 |
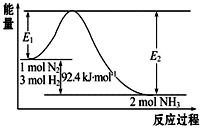 合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=Q kJ?mol-1,能量变化如图所示,回答下列问题:
合成氨工业的核心反应是:N2(g)+3H2(g)?2NH3(g)△H=Q kJ?mol-1,能量变化如图所示,回答下列问题: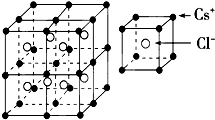 根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为
根据如图推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为