题目内容
元素A、B、C都是周期表中前18号元素,它们的原子序数相对大小为A<B<C,A元素原子的最外层电子数为次外层电子的二倍,B元素的原子次外层是最外层电子数的二倍,B和C可能形成共价化合物BC4.试指出
(1)这三种元素所对应的气态氢化物中最不稳定的是 (填化学式),该氢化物在空气中燃烧的化学方程式为 ;
(2)BC4的电子式是 .
(1)这三种元素所对应的气态氢化物中最不稳定的是
(2)BC4的电子式是
考点:位置结构性质的相互关系应用
专题:
分析:元素A、B、C都是周期表中前18号元素,它们的原子序数相对大小为A<B<C,A元素原子的最外层电子数为次外层电子的二倍,最外层电子数不超过8个,K层为最外层不超过2个,则A元素次外层为K层,则A原子核外电子数为6,所以A是C元素;
B元素的原子次外层是最外层电子数的二倍,且原子序数大于A,则B元素次外层电子数是8,所以B原子序数为14,则为Si元素;
B和C可能形成共价化合物BC4,且B的原子序数小于C,则C是Cl元素;
(1)元素的非金属性越弱,其气态氢化物越不稳定;硅烷在空气中燃烧生成二氧化硅和水;
(2)四氯化硅属于共价化合物,Si原子和每个Cl原子之间共用一对电子.
B元素的原子次外层是最外层电子数的二倍,且原子序数大于A,则B元素次外层电子数是8,所以B原子序数为14,则为Si元素;
B和C可能形成共价化合物BC4,且B的原子序数小于C,则C是Cl元素;
(1)元素的非金属性越弱,其气态氢化物越不稳定;硅烷在空气中燃烧生成二氧化硅和水;
(2)四氯化硅属于共价化合物,Si原子和每个Cl原子之间共用一对电子.
解答:
解:元素A、B、C都是周期表中前18号元素,它们的原子序数相对大小为A<B<C,A元素原子的最外层电子数为次外层电子的二倍,最外层电子数不超过8个,K层为最外层不超过2个,则A元素次外层为K层,则A原子核外电子数为6,所以A是C元素;
B元素的原子次外层是最外层电子数的二倍,且原子序数大于A,则B元素次外层电子数是8,所以B原子序数为14,则为Si元素;
B和C可能形成共价化合物BC4,且B的原子序数小于C,则C是Cl元素;
(1)元素的非金属性越弱,其气态氢化物越不稳定,这几种元素中非金属性最弱的是Si元素,则这三种元素所对应的气态氢化物中最不稳定的是SiH4;硅烷在空气中燃烧生成二氧化硅和水,反应方程式为SiH4+2O2
SiO2+2H2O,
故答案为:SiH4;SiH4+2O2
SiO2+2H2O;
(2)四氯化硅属于共价化合物,Si原子和每个Cl原子之间共用一对电子,其电子式为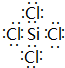 ,故答案为:
,故答案为: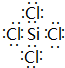 .
.
B元素的原子次外层是最外层电子数的二倍,且原子序数大于A,则B元素次外层电子数是8,所以B原子序数为14,则为Si元素;
B和C可能形成共价化合物BC4,且B的原子序数小于C,则C是Cl元素;
(1)元素的非金属性越弱,其气态氢化物越不稳定,这几种元素中非金属性最弱的是Si元素,则这三种元素所对应的气态氢化物中最不稳定的是SiH4;硅烷在空气中燃烧生成二氧化硅和水,反应方程式为SiH4+2O2
| ||
故答案为:SiH4;SiH4+2O2
| ||
(2)四氯化硅属于共价化合物,Si原子和每个Cl原子之间共用一对电子,其电子式为
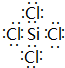 ,故答案为:
,故答案为: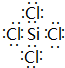 .
.
点评:本题考查位置结构性质的相互关系及应用,涉及电子式和方程式的书写、元素周期律等知识点,明确物质的结构、性质及元素周期律内涵即可解答,熟练掌握元素化合物知识,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
朱自清在《荷塘月色》中写道:“薄薄的青雾浮起在荷塘里…月光是隔了树照过来的,高处丛生的灌木,落下参差的斑驳的黑影…”月光穿过薄雾形成的种种美景的本质原因是( )
| A、空气中的小水滴颗粒直径大小约为1nm~100nm |
| B、光是一种胶体 |
| C、雾是一种胶体 |
| D、发生丁达尔效应 |
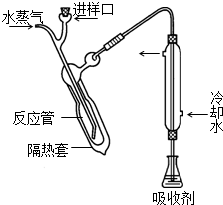 凯氏定氮法测定奶粉中蛋白质含量的步骤如下:
凯氏定氮法测定奶粉中蛋白质含量的步骤如下: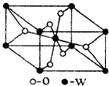 原子序数小于36的X、Y、Z、W四种元素,原子序数依次增大.其中X元素的一种核素的质量数为12,中子数为6; Y是空气中含量最多的元素;Z的基态原子核外5 个轨道上填充了电子,且有2个未成对电子;W的原子序数为22.
原子序数小于36的X、Y、Z、W四种元素,原子序数依次增大.其中X元素的一种核素的质量数为12,中子数为6; Y是空气中含量最多的元素;Z的基态原子核外5 个轨道上填充了电子,且有2个未成对电子;W的原子序数为22.
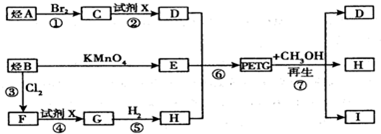 这种材料可采用如图所示的合成路线已知:(1)
这种材料可采用如图所示的合成路线已知:(1)