题目内容
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、通常状况下,1NA个H2分子占有的体积是22.4L |
| B、1mol氧是32g |
| C、摩尔是国际七个基本物理量之一 |
| D、常温常压下,2.12gNa2CO3固体中含有的CO32-离子数位0.02NA |
考点:阿伏加德罗常数,气体摩尔体积
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.通常状况下Vm≠22.4L/mol;
B.物质的类别指代不明;
C.摩尔是物质的量的单位;
D.质量转化为物质的量,结合碳酸钠的构成解答.
B.物质的类别指代不明;
C.摩尔是物质的量的单位;
D.质量转化为物质的量,结合碳酸钠的构成解答.
解答:
解:A.1NA个H2分子,物质的量为1mol,通常状况下Vm≠22.4L/mol,所以1NA个H2分子占有的体积不是22.4L,故A错误;
B.物质的类别指代不明,应指明具体的物质,故B错误;
C.摩尔是物质的量的单位,不是物理量,故C错误;
D.1个碳酸钠晶体中含有1个碳酸根离子,2.12gNa2CO3固体的物质的量=
=0.02mol,所以含有CO32-离子数=0.02mol×1×NA=0.02NA,故D正确;
故选:D.
B.物质的类别指代不明,应指明具体的物质,故B错误;
C.摩尔是物质的量的单位,不是物理量,故C错误;
D.1个碳酸钠晶体中含有1个碳酸根离子,2.12gNa2CO3固体的物质的量=
| 2.12g |
| 106g/mol |
故选:D.
点评:本题考查了阿伏伽德罗常数,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量、气体摩尔体积之间的转化关系是解题关键,注意物质的量使用注意事项.

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
0.1mol/L的Na2S溶液中,有关粒子的浓度大小关系正确的是( )
| A、c(Na+)+c(H+)=c(S2-)+c(HS-)+c(OH-) |
| B、c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
| C、c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| D、c(Na+)=2c(S2-)+2c(HS-)+c(H2S) |
在一定条件下,对于A2(g)+3B2(g)?2AB3(g)反应来说,下列所表示的化学反应速率中最大的是( )
| A、v(A2)=0.8mol?L-1?s-1 |
| B、v(A2)=40mol?L-1?min-1 |
| C、v(AB3)=1.0mol?L-1?s-1 |
| D、v(B2)=1.2mol?L-1?s-1 |
 如图所示,按如图甲装置进行实验,若图乙的x轴表示流入电极的电子的量,则y轴不可能表示的是( )
如图所示,按如图甲装置进行实验,若图乙的x轴表示流入电极的电子的量,则y轴不可能表示的是( )| A、c(Ag+) |
| B、c(NO3-) |
| C、溶液的pH |
| D、铁片质量 |
下列说法正确的是( )
| A、某种液体的饱和蒸气压与温度有关 |
| B、物体内所有分子热运动动能的总和就是物体的内能 |
| C、气体的温度升高,每个分子的动能都增大 |
| D、不是所有晶体都具有各向异性的特点 |
下列实验操作,能有效改变反应速率且达到变化要求的是( )
| A、为增大泡沫灭火器中Al2(SO4)3与小苏打的反应速率,改用小苏打和苏打的混合物 |
| B、为加快盐酸和锌制取氢气的速率又不减少氢气的量,可加少量硝酸银溶液 |
| C、在稀硫酸和铁粉反应制取氢气时,为减慢反应速率,可以加入适量醋酸钠 |
| D、用3 mL乙醇、2 mL浓H2SO4、2 mL冰醋酸制乙酸乙酯,为增大反应速率,可改用6 mL乙醇、4 mL浓H2SO4、4 mL冰醋酸 |
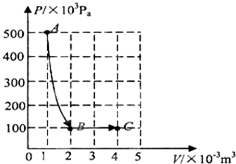 一定质量的理想气体,经过如图所示的由A经B到C的状态变化.设状态A的温度为400K.求:
一定质量的理想气体,经过如图所示的由A经B到C的状态变化.设状态A的温度为400K.求: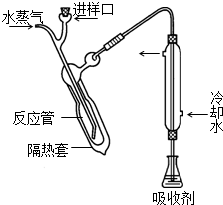 凯氏定氮法测定奶粉中蛋白质含量的步骤如下:
凯氏定氮法测定奶粉中蛋白质含量的步骤如下: