题目内容
4.NA代表阿伏伽德罗常数的值.下列说法正确的是( )| A. | 在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA | |
| B. | 含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间 | |
| C. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA | |
| D. | 用惰性电极电解饱和碳酸钠溶液时,电路上通过2mol电子时产生气体分子总数为NA |
分析 A、求出丁烷的物质的量,然后根据丁烷中含10条极性共价键来分析;
B、氧化钠和过氧化钠均由2个钠离子和1个阴离子构成;
C、5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物和还原产物均为氮气,且4mol氮气中的8mol氮原子中有5mol为氧化产物,3mol为还原产物;
D、用惰性电极电解饱和碳酸钠溶液时,实际上是电解水.
解答 解:A.在0℃、101kPa条件下,11.2L丁烷的物质的量为0.5mol,其中含极性共价键(C-H)的物质的量为0.5mol×10=5mol,故A正确;
B.根据钠原子守恒,含23g钠元素的Na2O和Na2O2混合物的物质的量为0.5mol,而氧化钠和过氧化钠均由2个钠离子和1个阴离子构成,故其中阴离子数目为0.5NA,故B错误;
C.5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物和还原产物均为氮气,其中氧化产物与还原产物的物质的量之比为5:3,当氧化产物比还原产物每多14g时,共生成氮气2mol,转移电子数为7.5NA,故C错误;
D.用惰性电极电解饱和碳酸钠溶液,相当于电解水,当电路上通过2mol电子时产生1molH2,0.5molO2,分子总数为1.5NA,故D错误;
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案
相关题目
14.保护环境已成为人类的共识,人类应以可持续发展的方式使用资源,以合理的方式发现进行处理并循环使用.下列做法不利于环境保护的是( )
| A. | 发电厂的煤经脱硫处理 | |
| B. | 将煤汽化作燃料 | |
| C. | 回收并合理处理聚乙烯塑料废物 | |
| D. | 电镀废液(其中含重金属盐的离子)经中和后直接排放 |
19.将过氧化钠投入FeCl2溶液中,可观察到的实验现象是( )
| A. | 有白色沉淀生成 | B. | 没有沉淀生成 | ||
| C. | 有红褐色沉淀生成 | D. | 有无色气体产生 |
9.表是A、B、C、D、E五种有机物的有关信息:
根据表中信息回答下列问题:
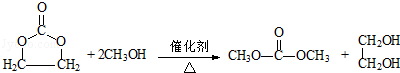
(1)A与溴水反应的生成物的名称叫做1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式: .
.
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH 2n+2.当n=5时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤任何条件下不与氢气反应 ⑥可使酸性高锰酸钾溶液和溴水均褪色写出在浓硫酸作用下,B与浓硝酸反应的化学方程式: ;
;
(4)写出由C氧化生成D的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
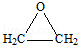
| A | ①能使溴的四氯化碳溶液褪色 ②比例模型如图  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成 ②球棍模型如图 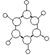 |
| C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
(1)A与溴水反应的生成物的名称叫做1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式:
 .
.(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH 2n+2.当n=5时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号).
①无色无味液体 ②有毒 ③不溶于水 ④密度比水大 ⑤任何条件下不与氢气反应 ⑥可使酸性高锰酸钾溶液和溴水均褪色写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:
 ;
;(4)写出由C氧化生成D的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O.
16.将过量SO2通入下列溶液中,能出现白色浑浊的是( )
①Ca(OH)2;
②BaCl2;
③NaAlO2;
④Na2SiO3;
⑤Ba(NO3)2;
⑥苯酚钠;
⑦Na2CO3.
①Ca(OH)2;
②BaCl2;
③NaAlO2;
④Na2SiO3;
⑤Ba(NO3)2;
⑥苯酚钠;
⑦Na2CO3.
| A. | ①②④⑦ | B. | ②③⑥⑦ | C. | ④⑤⑥⑦ | D. | ④⑤⑥ |
13.下列实验的操作和所用的试剂都正确的是( )
| A. | 要检验己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| B. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| C. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 | |
| D. | 除去乙酸乙酯中少量的乙酸,可以加氢氧化钠溶液后分液 |

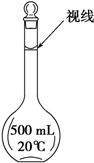 实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol/L的FeSO4溶液,实验操作步骤有:
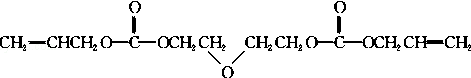
 .
. .
.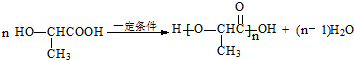 .
.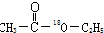 的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.