题目内容
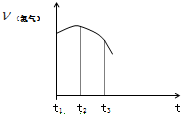 把除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是
把除去氧化膜的镁条投入到盛有稀盐酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:金属镁与酸的反应为放热反应,从曲线的变化判断影响反应速率的因素.
解答:
解:金属镁与酸的反应为放热反应,反应开始时,温度不断升高,则反应速率逐渐增大,但随着反应的极性,反应物的浓度逐渐降低,此时浓度的影响大于温度的影响,反应速率反而减小,氧化镁与盐酸反应生成氯化镁和水,反应方程式为MgO+2HCl=MgCl2+H2O.
故答案为:镁条与盐酸的反应是放热反应,溶液温度升高,反应速率加快;盐酸浓度减小,反应速率减慢;MgO+2HCl=MgCl2+H2O.
故答案为:镁条与盐酸的反应是放热反应,溶液温度升高,反应速率加快;盐酸浓度减小,反应速率减慢;MgO+2HCl=MgCl2+H2O.
点评:本题是考查化学反应速率图象的题目,题目难度不大,注意t2~t3速率变化的主要原因为易错点,把握影响反应速率的因素.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
能用如图气体制取装置制取少量气体并能“随开随用、随关随停”的是( )
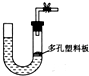

| A、大理石和稀硫酸制取二氧化碳 |
| B、锌粒和稀硫酸制氢气 |
| C、浓盐酸和二氧化锰制取氯气 |
| D、过氧化钠和水制取氧气 |
有关糖类物质概念的叙述中,正确的是( )
| A、糖类是具有甜味的物质 |
| B、糖类是具有Cn(H2O)m通式的物质 |
| C、葡萄糖是一种单糖的主要原因是一种多羟基醛 |
| D、淀粉是一种白色粉末,本身没有甜味 |
将如图所示实验装置的K闭合,下列判断正确的是( )
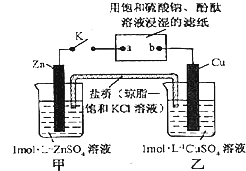

| A、片刻后可观察到滤纸b点变红色 |
| B、电子沿Zn→a→b→Cu路径流动 |
| C、片刻后甲池中c(SO42-)增大 |
| D、Cu电极上发生还原反应 |
主族元素单质及化合物在许多性质上都存在着递变规律.下列有关说法不正确的是( )
| A、卤化银的颜色按AgCl、AgBr、AgI 的顺序依次加深 |
| B、氧族元素氢化物稳定性按H2O、H2S、H2Se、H2Te的顺序依次减小 |
| C、氢化物的沸点按NH3、BiH3、SbH3、AsH3、PH3的顺序依次递减 |
| D、最高价氧化物对应水化物碱性按NaOH、KOH、RbOH、CsOH的顺序依次增强 |