题目内容
11.写出下列各组混和物的分离或提纯采用的方法(1)分离碘水中的碘单质:萃取;
(2)分离水和植物油的混合物:分液;
(3)除去食盐溶液中的水:蒸发;
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)的混合物:蒸馏;
(5)分离饱和氯化钾溶液和沙子的混合物:过滤.
分析 (1)碘不易溶于水,易溶于有机溶剂;
(2)水和植物油分层;
(3)食盐溶于水,水易挥发;
(4)酒精与甲苯互溶,但沸点不同;
(5)沙子不溶于水.
解答 解:(1)碘不易溶于水,易溶于有机溶剂,则利用萃取分离,故答案为:萃取;
(2)水和植物油分层,则利用分液分离,故答案为:分液;
(3)食盐溶于水,水易挥发,则利用蒸发除去食盐溶液中的水,故答案为:蒸发;
(4)酒精与甲苯互溶,但沸点不同,则利用蒸馏分离,故答案为:蒸馏;
(5)沙子不溶于水,则利用过滤分离饱和氯化钾溶液和沙子,故答案为:过滤.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
1.用NA表示阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,11.2 L SO3中含有0.5NA个SO3分子 | |
| B. | 48g O3气体含有3NA个氧原子 | |
| C. | 在1L0.5mol•L-lFeCl3溶液中含有0.5NA个Fe3+ | |
| D. | 1.5 mol NO2与足量水反应,转移的电子数为1.5NA |
2.常温下,下列物质的水溶液,因为水解使溶液的pH<7的是( )
| A. | Na2S | B. | H2SO3 | C. | Al(SO4)3 | D. | NaHSO4 |
6.实验室中配制250mL 0.10mo1•L-1NaOH溶液时,必须使用到的玻璃仪器是( )
| A. | 锥形瓶 | B. | 试管 | C. | 分液漏斗 | D. | 250mL容量瓶 |
16.反应4P+3KOH+3H2O═3KH2PO2+PH3中磷单质发生的变化是( )
| A. | 只被氧化 | B. | 被氧化与被还原的个数比为1:3 | ||
| C. | 只被还原 | D. | 氧化剂与还原剂的质量比是1:3 |
1.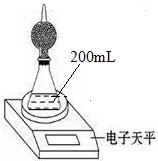 如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
①反应中生成气体的质量为1.2g.
②试计算样品中铝的质量分数?(写出计算过程)
③求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度?(写出计算过程)
 如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:
如图是测定铝粉(含铜粉等杂质不与酸反应)的纯度的实验装置.装置为干燥管和锥形瓶,干燥管内装有氯化钙,锥形瓶内所用的硫酸(足量)的物质的量浓度为4mol•L-1.不同时间电子天平的读数如下表所示:| 实验操作 | t/min | 电子天平的读数/g |
| 装置+硫酸溶液 | 320.0 | |
| 装置+硫酸溶液+样品 | 0 | 335.0 |
| 1 | 334.5 | |
| 2 | 334.1 | |
| 3 | 333.8 | |
| 4 | 333.8 |
②试计算样品中铝的质量分数?(写出计算过程)
③求反应后锥形瓶内硫酸溶液(溶液的体积变化忽略)的物质的量的浓度?(写出计算过程)