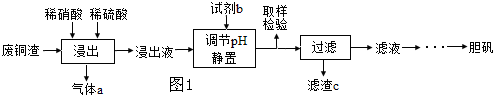
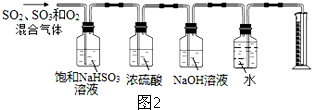
题目内容
下列装置所示的实验不能达到目的是( )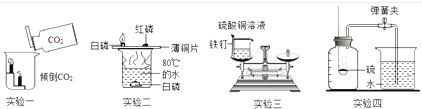

| A、实验一:验证二氧化碳密度大于空气,不支持燃烧 |
| B、实验二:探究燃烧需要的条件 |
| C、实验三:探究质量守恒定律 |
| D、实验四:测量空气中氧气所占的体积分数 |
考点:化学实验方案的评价
专题:
分析:A.下面的蜡烛先熄灭;
B.可以看到烧杯中的白磷和铜片上的红磷不燃烧,铜片上的白磷燃烧;
C.用铁和硫酸铜的反应前后质量不变;
D.测定空气中氧气的含量所选用的物质与氧气反应不能生成气体.
B.可以看到烧杯中的白磷和铜片上的红磷不燃烧,铜片上的白磷燃烧;
C.用铁和硫酸铜的反应前后质量不变;
D.测定空气中氧气的含量所选用的物质与氧气反应不能生成气体.
解答:
解:A.向盛有阶梯蜡烛的烧杯中倒入二氧化碳能证明二氧化碳的密度比空气大和不支持燃烧的性质,故A正确;
B.使用实验二的装置,可以看到烧杯中的白磷和铜片上的红磷不燃烧,铜片上的白磷燃烧,能用来探究燃烧的条件,能达到实验的目的,故B正确;
C.使用铁和硫酸铜的反应能用来探究质量守恒定律,故C正确;
D.使用硫燃烧生成的是二氧化硫,不能用来测量空气中氧气的含量,故D错误.
故选D.
B.使用实验二的装置,可以看到烧杯中的白磷和铜片上的红磷不燃烧,铜片上的白磷燃烧,能用来探究燃烧的条件,能达到实验的目的,故B正确;
C.使用铁和硫酸铜的反应能用来探究质量守恒定律,故C正确;
D.使用硫燃烧生成的是二氧化硫,不能用来测量空气中氧气的含量,故D错误.
故选D.
点评:本题考查了常见的实验装置与实验目的关系,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
下列物质的体积一定是22.4 L的是( )
| A、标准状况下18g水 |
| B、17g氨气 |
| C、标准状况下44g二氧化碳 |
| D、常温常压下2g氢气 |
反应2SO2+O2?2SO3经过一段时间后,O2的浓度增加了0.2mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L?s),则这段时间为( )
| A、0.1 s |
| B、2.5 s |
| C、5 s |
| D、10 s |
只用一种试剂就能鉴别出NH4Cl、Na2SO4、(NH4)2SO4、三种溶液(允许加热),应选择( )
| A、BaCl2 |
| B、HCl |
| C、NaOH |
| D、Ba(OH)2 |