题目内容
下列物质的体积一定是22.4 L的是( )
| A、标准状况下18g水 |
| B、17g氨气 |
| C、标准状况下44g二氧化碳 |
| D、常温常压下2g氢气 |
考点:气体摩尔体积
专题:
分析:A、标准状况水不是气体;
B、温度压强不知不能计算气体体积;
C、依据n=
=
计算物质的量得到气体体积;
D、常温常压下1mol气体体积不是22.4L;
B、温度压强不知不能计算气体体积;
C、依据n=
| m |
| M |
| V |
| 22.4 |
D、常温常压下1mol气体体积不是22.4L;
解答:
解:A、18g水物质的量为1mol,标准状况水不是气体,体积不是22.4L,故A错误;
B、温度压强不知不能计算气体体积,故B错误;
C、依据n=
=
=1mol,n=
计算物质的量得到气体体积22.4L,故C正确;
D、常温常压下1mol气体体积不是22.4L,故D错误;
故选C.
B、温度压强不知不能计算气体体积,故B错误;
C、依据n=
| m |
| M |
| 44g |
| 44g/mol |
| V |
| 22.4 |
D、常温常压下1mol气体体积不是22.4L,故D错误;
故选C.
点评:本题考查了气体摩尔体积条件的应用分析,主要是物质状态、温度压强的分析应用,掌握基础是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列叙述正确的是( )
| A、交叉分类法和树状分类法是化学上仅有的两种分类方法 |
| B、化合物中某元素处于最高价只能被还原 |
| C、H2SO4在电流作用下在水中电离出H+和SO42- |
| D、偏二甲肼(分子式:C2H8N2)是一种有机高能燃料,它的摩尔质量为60g |
下列溶液中的c(Cl-) 与150mL、1mol/LAlCl3 溶液中的c(Cl-) 相等的是( )
| A、150 mL、1 mol/L NaCl溶液 |
| B、25 mL、3 mol/L NH4Cl 溶液 |
| C、75 mL、2 mol/L MgCl2溶液 |
| D、75 mL、2 mol/L FeCl3溶液 |
下列装置所示的实验不能达到目的是( )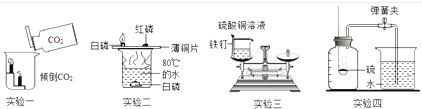

| A、实验一:验证二氧化碳密度大于空气,不支持燃烧 |
| B、实验二:探究燃烧需要的条件 |
| C、实验三:探究质量守恒定律 |
| D、实验四:测量空气中氧气所占的体积分数 |
下列萃取与分液相结合进行的操作(用苯从碘水中萃取碘单质,且已知苯的密度比水小)中错误的是( )
| A、碘水和苯加入分液漏斗后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡,并不时地放气 |
| B、静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体) |
| C、打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出,及时关闭活塞 |
| D、最后继续打开活塞,另用烧杯在分液漏斗的下口承接并保存上层液体 |