题目内容
火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652kJ的热量.
(1)反应的热化学方程式为 ;
(2)又已知H2O(l)=H2O(g);△H=+44kJ/mol,则16g液态肼和液态双氧水反应生成液态水时放出的热量是 ;
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体外还有一个很大的优点是 .
(1)反应的热化学方程式为
(2)又已知H2O(l)=H2O(g);△H=+44kJ/mol,则16g液态肼和液态双氧水反应生成液态水时放出的热量是
(3)此反应用于火箭推进,除释放大量的热和快速产生大量气体外还有一个很大的优点是
考点:热化学方程式
专题:化学反应中的能量变化
分析:(1)反应方程式为:N2H4+2H2O2=N2+4H2O,根据0.4mol液态肼放出的热量,计算1mol液态肼放出的热量,进而写出热化学方程式;
(2)结合上述写出的热化学方程式和谁转化的热化学方程式,根据盖斯定律合并写出生成液态水时的热化学方程式进行计算;
(3)依据反应N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)的产物是氮气和水分析该反应的优点.
(2)结合上述写出的热化学方程式和谁转化的热化学方程式,根据盖斯定律合并写出生成液态水时的热化学方程式进行计算;
(3)依据反应N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)的产物是氮气和水分析该反应的优点.
解答:
解:(1)反应方程式为:N2H4+2H2O2═N2+4H2O,0.4mol液态肼放出256.652KJ的热量,则1mol液态肼放出的热量为
=641.63kJ,
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63kJ/mol,
故答案为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63kJ/mol;
(2)①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63kJ/mol;
②H2O(g)=H2O(l)△H=-44kJ/mol;
依据盖斯定律①+②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l);△H=-817.63kJ/mol;
热化学方程式中32g全部反应放热817.63kJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量为:817.63kJ×
=408.815kJ,
故答案为:408.815kJ;
(3)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,清洁无污染,
故答案为:产物无污染.
| 265.65kJ |
| 0.4 |
所以反应的热化学方程式为:N2H4(g)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63kJ/mol,
故答案为:N2H4(g)+2H2O2(l)=N2(g)+4H2O(g)△H=-641.63kJ/mol;
(2)①N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-641.63kJ/mol;
②H2O(g)=H2O(l)△H=-44kJ/mol;
依据盖斯定律①+②×4得到:N2H4(l)+2H2O2(l)═N2(g)+4H2O(l);△H=-817.63kJ/mol;
热化学方程式中32g全部反应放热817.63kJ,16g液态肼与足量双氧水反应生成氮气和液态水时,放出的热量为:817.63kJ×
| 1 |
| 2 |
故答案为:408.815kJ;
(3)还原剂肼(N2H4)和强氧化剂H2O2,当它们混合时,即产生大量的氮气和水蒸气,除释放大量热量和快速产生大量气体外,还有很突出的优点是,产物为氮气和水,清洁无污染,
故答案为:产物无污染.
点评:本题考查了热化学方程式的书写、有关反应热的计算,题目难度中等,注意盖斯定律的应用,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
下列装置所示的实验不能达到目的是( )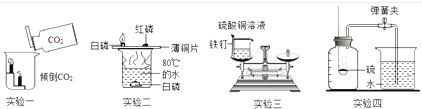

| A、实验一:验证二氧化碳密度大于空气,不支持燃烧 |
| B、实验二:探究燃烧需要的条件 |
| C、实验三:探究质量守恒定律 |
| D、实验四:测量空气中氧气所占的体积分数 |
下列过程中的焓变小于零的是( )
| A、石灰石高温分解 |
| B、氢氧化钡晶体与氯化铵晶体反应 |
| C、二氧化碳与碳反应 |
| D、铝与盐酸反应 |
下列萃取与分液相结合进行的操作(用苯从碘水中萃取碘单质,且已知苯的密度比水小)中错误的是( )
| A、碘水和苯加入分液漏斗后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡,并不时地放气 |
| B、静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体) |
| C、打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出,及时关闭活塞 |
| D、最后继续打开活塞,另用烧杯在分液漏斗的下口承接并保存上层液体 |
在pH都等于9的KOH和CH3COOK两种溶液中,设由水电离产生的OH-离子浓度分别为Xmol/L与Ymol/L,则X和Y的关系为( )
| A、X=Y |
| B、Y=10-4 X |
| C、X=10-4 Y |
| D、X>Y |
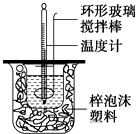 用50mL 0.50mol?L-1的盐酸与50mL 0.55mol?L-1的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
用50mL 0.50mol?L-1的盐酸与50mL 0.55mol?L-1的氢氧化钠溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题.