题目内容
化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子.则
(1)X元素基态原子的电子排布式是 ,Y原子的价电子轨道表示式是 .
(2)YX2的分子构型是 .
(3)YX2分子中,Y原子的杂化类型是 ,一个YX2分子中含 个π键.
(1)X元素基态原子的电子排布式是
(2)YX2的分子构型是
(3)YX2分子中,Y原子的杂化类型是
考点:位置结构性质的相互关系应用,共价键的形成及共价键的主要类型,原子轨道杂化方式及杂化类型判断
专题:原子组成与结构专题,元素周期律与元素周期表专题,化学键与晶体结构
分析:化合物YX2、ZX2中X、Y、Z都是前三周期元素,X原子最外能层的p能级中有一个轨道填充了2个电子,则X的最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,然后结合元素化合物性质、物质的结构来分析解答.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,然后结合元素化合物性质、物质的结构来分析解答.
解答:
解:化合物YX2、ZX2中X、Y、Z都是前三周期元素,X原子最外能层的p能级中有一个轨道填充了2个电子,则X的最外层电子排布式为ns2np4,为第VIA族元素;
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,
(1)X是O元素,原子序数为8,其最外层有6个电子,所以O的电子排布式为1s22s22p4,Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,Y原子的价电子轨道表示式为 故答案为:1s22s22p2;
故答案为:1s22s22p2; ;
;
(2)YX2的结构式为O=C=O,C为sp杂化,分子构型为直线型,故答案为:直线型;
(3)YX2分子中,结构式为O=C=O及直线结构可知,由Y原子的杂化类型是sp杂化,双键中有1个π键,则一个YX2分子中含2个π键,故答案为:sp杂化;2.
Y原子的最外层中p能级的电子数等于前一能层电子总数,p能级最多排列6个电子,则Y次外层为K层,Y原子最外层p能级上电子数是2,Y原子含有6个电子,为C元素,XX与Y同周期,Y与Z同主族,所以X是O元素,Z为Si元素,
(1)X是O元素,原子序数为8,其最外层有6个电子,所以O的电子排布式为1s22s22p4,Y是C原子,根据构造原理知,其核外电子排布式为:1s22s22p2,Y原子的价电子轨道表示式为
 故答案为:1s22s22p2;
故答案为:1s22s22p2; ;
;(2)YX2的结构式为O=C=O,C为sp杂化,分子构型为直线型,故答案为:直线型;
(3)YX2分子中,结构式为O=C=O及直线结构可知,由Y原子的杂化类型是sp杂化,双键中有1个π键,则一个YX2分子中含2个π键,故答案为:sp杂化;2.
点评:本题考查位置、结构、性质的关系及应用,为高频考点,把握原子中电子排布及分子结构为解答的关键,侧重分析、推断能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 如图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标,这里的钙、镁、钾、钠是指( )
如图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标,这里的钙、镁、钾、钠是指( )| A、元素 | B、原子 | C、单质 | D、分子 |
下列溶液一定呈中性的是( )
| A、pH=7的溶液 | ||
B、c(OH-)=
| ||
| C、使石蕊试液呈紫色的溶液 | ||
| D、c(H+)=10-7mol/L的溶液 |
下列叙述正确的是( )
| A、交叉分类法和树状分类法是化学上仅有的两种分类方法 |
| B、化合物中某元素处于最高价只能被还原 |
| C、H2SO4在电流作用下在水中电离出H+和SO42- |
| D、偏二甲肼(分子式:C2H8N2)是一种有机高能燃料,它的摩尔质量为60g |
下列装置所示的实验不能达到目的是( )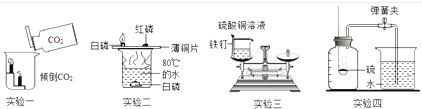

| A、实验一:验证二氧化碳密度大于空气,不支持燃烧 |
| B、实验二:探究燃烧需要的条件 |
| C、实验三:探究质量守恒定律 |
| D、实验四:测量空气中氧气所占的体积分数 |