题目内容
2.将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是( )| A. | NaOH、NaCl、NaAlO2 | B. | KNO3、NaCl、CH3COONa | ||
| C. | Na2S、(NH4)2SO3、AgNO3 | D. | Ba(NO3)2、FeSO4、NH4HCO3 |
分析 A.盐酸与氢氧化钠、偏铝酸钠都能发生反应;
B.盐酸不与硝酸钾、氯化钠反应,只与醋酸钠反应;
C.盐酸与三种物质都发生反应;
D.盐酸与碳酸氢铵反应,酸性条件下硝酸根具有强氧化性,可以氧化亚铁离子.
解答 解:A.存在反应有:NaOH+2HCl=NaCl+H2O、NaAlO2+4HCl=AlCl3+NaCl+2H2O,故A不选;
B.加入稀盐酸后只发生反应CH3COONa+HCl=CH3COOH+NaCl,故B选;
C.存在反应:HCl+AgNO3=AgCl↓+HNO3、2HCl+(NH4)2SO3=2NH4Cl+H2O+SO2↑、HCl+Na2S=2HCl+H2S,故C不选;
D.存在NH4HCO3+HCl=NH4Cl+H2O+CO2↑、4H++NO3-+3Fe2+=3Fe3++NO↑+2H2O、Ba2++SO42-=BaSO4↓,故D不选;
故选B.
点评 本题考查常见元素及其化合物性质、离子反应发生条件,题目难度中等,明确常见化合物性质为解答关键,注意熟练掌握离子反应发生条件,试题培养了学生的灵活应用能力.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
13.下列有关sp杂化轨道的叙述正确的是( )
| A. | 是由一个1s轨道和一个2p轨道线性组合而成 | |
| B. | 等性sp杂化轨道中所含s、p的成分一样 | |
| C. | 等性sp杂化轨道有两个,一个能量升高,另一个能量降低,但总能量保持不变 | |
| D. | sp杂化轨道可与其他原子轨道形成σ键和π键 |
10.丙烯醛(结构简式为CH2=CH-CHO)能发生的化学反应有( )
①加成 ②消除(消去) ③取代 ④氧化 ⑤还原 ⑥加聚 ⑦缩聚.
①加成 ②消除(消去) ③取代 ④氧化 ⑤还原 ⑥加聚 ⑦缩聚.
| A. | ①③⑤⑦ | B. | ②④⑥ | C. | ①④⑤⑥ | D. | ③④⑤⑥ |
17.高炉炼铁中生成铁的反应一定是( )
| A. | 氧化还原反应 | B. | 置换反应 | C. | 复分解反应 | D. | 分解反应 |
7.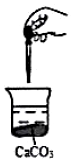 如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
 如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )
如图,向烧杯中滴加几滴浓盐酸,CaCO3固体还有剩余(忽略体积、温度的变化),下列数值变小的是( )| A. | c(Ca2+) | B. | c(CO32-) | C. | c(H+) | D. | c(碳酸钙的溶解度) |
14.下列物质的性质可以用“键能”来解释的是( )
| A. | SiO2熔点高 | B. | 氩气性质稳定 | C. | 碘易升华 | D. | NH3极易溶于水 |
11.下列溶液中通入SO2一定不会产生沉淀的是( )
| A. | Ba(OH)2 | B. | Na2S | C. | Ba(NO3)2 | D. | BaCl2 |
12.与HCl比,HI( )
| A. | 颜色更深 | B. | 沸点更低 | C. | 还原性更强 | D. | 稳定性更强 |
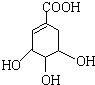 莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下:
莽草酸是合成治疗禽流感的药物--达菲(Tamiflu)的原料之一.莽草酸是A的一种异构体.A的结构简式如下: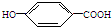 ),其反应类型是消去反应,化学方程式是
),其反应类型是消去反应,化学方程式是 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$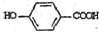 +2H2O.
+2H2O. .
.