题目内容
16.在一定条件下的定容密闭容器中,下列说法能表明反应A(s)+2B(g)═C(g)+D(g) 已达平衡状态的是( )| A. | 混合气体的压强不再改变 | |
| B. | 单位时间内生成n mol A的同时,生成2n mol的B | |
| C. | C的生成速率是B 的生成速率的两倍 | |
| D. | 混合气体的密度不再改变 |
分析 A、反应物A(s)是固体,反应两边气体化学计量数相等,压强始终相等;
B、都体现有逆反应方向;
C、只要反应发生就有C的生成速率是B 的生成速率的两倍;
D、混合气体的密度不再改变,说明气体的质量不变反应达平衡状态.
解答 解:A、由于A是固态,反应前后的气体的化学计量数之和都是2,故压强始终不变,故A错误;
B、都体现有逆反应方向,未体现正与逆的关系,故B错误;
C、只要反应发生就有C的生成速率是B 的生成速率的两倍,所以不一定是平衡状态,故C错误;
D、混合气体的密度不再改变,说明气体的质量不变反应达平衡状态,故D正确;
故选D.
点评 本题考查化学平衡状态的判断,做题时注意反应两边气体的化学计量数是否相等,若相等,压强、物质的量、体积会始终不变;还要注意物质的状态,本题难度中等.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案
相关题目
6.在一定条件下,向2L恒容密闭容器中加入2mol X、2mol Y.发生如下反应:
X(g)+Y(g)?Z(g);△H=-a kJ•mol-1(a>0).
经50s达平衡,此时Y的物质的量为1.2mol.下列说法错误的是( )
X(g)+Y(g)?Z(g);△H=-a kJ•mol-1(a>0).
经50s达平衡,此时Y的物质的量为1.2mol.下列说法错误的是( )
| A. | 用Z表示的化学反应速率为0.016 mol•L-1•s-1 | |
| B. | 恒温恒容下,通入Ne气,增大压强,Y的浓度不减小 | |
| C. | 恒温恒容下,再充入一定量的Z,重新达到平衡时,X的物质的量分数减小 | |
| D. | 达平衡后,实际放出的热量为b kJ,则b=a |
7.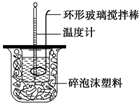 测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
 测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.某兴趣小组的实验数值结果大于57.3kJ•mol-1(中和热),原因可能是( )| A. | 实验装置中小烧杯杯中低于大烧杯杯口 | |
| B. | 用浓硫酸代替了稀硫酸 | |
| C. | 分多次把NaOH溶液倒入盛有硫酸的小烧杯中 | |
| D. | 用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度 |
11.下列能说明氯元素的非金属性比硫元素强的事实是( )
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子最外层有7个电子,S原子最外层有6个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子最外层有7个电子,S原子最外层有6个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS.
| A. | ①②④⑤ | B. | ①②③⑥ | C. | ①③⑤⑥ | D. | ①③④⑥ |
1.下列化学用语表达正确的是( )
| A. | HF的电子式为: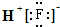 | B. | HClO的结构式:H-Cl-O | ||
| C. | CO2的电子式为: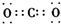 | D. | Cl-的结构示意图: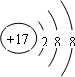 |
5. 有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
 有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )
有机物X由C、H、O三种元素组成,其分子结构模型如图所示(图中球与球之间连线表示单键或双键).关于该有机物叙述正确的是( )| A. | 分子中含有3种官能团 | |
| B. | 1 mol该有机物与足量溴水反应最多消耗3molBr2 | |
| C. | 1 mol该有机物最多能与2 mol NaOH反应 | |
| D. | 该有机物若能使酸性KMnO4溶液褪色,则可证明其分子中存在碳碳双键 |
6.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,现象和有关数据如图所示(气体体积数据已换算成标准状况).关于该固体混合物,下列说法正确的是( )


| A. | 含4.5gAl | |
| B. | 一定不含FeCl2,可能含有MgCl2和AlCl3 | |
| C. | 含有物质的量相等的(NH4)2SO4和MgCl2 | |
| D. | 含有MgCl2和FeCl2 |
