题目内容
表示0.1mol/L NaHCO3溶液中有关粒子浓度的关系正确的是 ( )
| A、c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-) |
| B、c(Na+)+c(H+)=c(OH-)+c(HCO3-)+c(CO32-) |
| C、c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| D、c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:NaHCO3溶液呈碱性,溶液中HCO3-水解程度大于HCO3-电离程度,结合溶液中物料守恒和电荷守恒解答该题.
解答:
解:A.NaHCO3溶液呈碱性,则应有c(OH-)>c(H+),故A错误;
B.溶液存在电荷守恒,即c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故B错误;
C.溶液存在电荷守恒,即c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D.溶液存在物料守恒,即c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故D正确;
故选CD.
B.溶液存在电荷守恒,即c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故B错误;
C.溶液存在电荷守恒,即c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D.溶液存在物料守恒,即c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3),故D正确;
故选CD.
点评:本题考查离子浓度的大小比较,为高频考点,把握盐类水解的原理为解答的关键,注意从守恒的角度比较离子浓度大小是常用的方法,题目难度中等.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
下列装置用于实验室以硫酸铝制取一定量Al2O3,能达到实验目的是 ( )
A、 称取样品 |
B、 样品溶解 |
C、 氢氧化铝沉淀过滤 |
D、 灼烧氢氧化铝沉淀 |
某实验需要470mL0.4mol?L-1NaOH溶液,配制该溶液时,用托盘天平称取NaOH固体的质量应为( )
| A、8.0g | B、7.5g |
| C、4.0g | D、7.52g |
能正确表示下列反应的离子方程式是( )
| A、铝与氢氧化钠溶液反应:2Al+2 OH-=2AlO2-+3H2O |
| B、将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O |
| C、用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O |
| D、过氧化钠溶于盐酸:Na2O2+2H+=2Na++2H2O |
下列离子方程式正确的是( )
| A、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| B、过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O |
| C、等体积、等物质的量浓度的NaHCO3和 Ba(OH)2两溶液混合:2HCO3-+Ba2++2OH-═BaCO3↓+CO32-+2H2O |
| D、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+═2Mn2++5NO3-+3H2O |
下列除去杂质的方法中,正确的是( )
| A、除去KCl溶液中的少量MgCl2,加入适量NaOH溶液,过滤 |
| B、除去FeSO4溶液中少量的CuSO4,加入足量铁屑,充分反应后过滤 |
| C、除去CO2中的少量HCl,通入足量的Na2CO3溶液,收集气体 |
| D、除去N2中的少量O2,通过灼热的炭层,收集气体 |



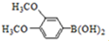 与化合物
与化合物 在一定条件可发生类似反应①的反应,其产物的结构简式为
在一定条件可发生类似反应①的反应,其产物的结构简式为