题目内容
15.能够说明苯分子中不存在单、双键,而是所有碳碳键完全相同的事实是( )| A. | 甲苯无同分异构体 | |
| B. | 邻二甲苯只有一种 | |
| C. | 苯分子中各原子均在一个平面内,各键键角均为120° | |
| D. | 1mol苯最多只能与3mol H2加成 |
分析 A、无论苯分子中碳碳键是否单双建交替,甲苯都无同分异构体;
B、如果是单双键交替结构,苯的邻二甲苯应有两种同分异构体,但实际上只有一种结构,能说明苯环结构中的化学键只有一种;
C、苯分子中各原子均在一个平面内,各键键角均为120°,说明苯为平面正六边形结构;
D、苯能和氢气加成,恰恰不能说明苯不是单双键交替的结构.
解答 解:A、无论苯分子中碳碳键是否单双建交替,甲苯都无同分异构体,所以不能说明苯分子中的碳碳键不是单、双键交替,故A不选;
B、如果是单双键交替结构,苯的邻二甲苯应有两种同分异构体,但实际上只有一种结构,能说明苯环结构中的化学键只有一种,不存在C-C单键与C=C双键的交替结构,故B正确;
C、苯分子中各原子均在一个平面内,各键键角均为120°,说明苯为平面正六边形结构,即苯中的6条碳碳键键完全相同,不是单双键交替的结构,故C正确;
D、苯能和氢气加成,说明苯中有不饱和度,恰恰不能说明苯不是单双键交替的结构,故D错误.
故选BC.
点评 本题考查苯的结构与性质,题目难度不大,注意掌握苯的结构,试题综合性较大,要求学生知识掌握全面,能运用知识分析和解决问题,重在能力的考查.

练习册系列答案
相关题目
8.已知元素R的某种同位素的氯化物RClx为离子化合物,R离子核内中子数为y个,核外电子数为z个,则该同位素的符号应表示为( )
| A. | ${\;}_{x}^{y}$R | B. | ${\;}_{z}^{y+x}$R | C. | ${\;}_{x+z}^{y}$R | D. | ${\;}_{x+z}^{y+x+z}$R |
6.室温下,向10mL 0.1mol/L NaOH溶液中加入0.1mol•L-1的一元酸 HA溶液pH的变化曲线如图所示(横坐标单位是mL).下列说法不正确的是( )
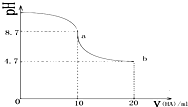

| A. | a点所示溶液中有c(Na+)>c(A-)>c(HA)>c(H+) | |
| B. | a、b两点曲线之间某时刻的溶液中有c(Na+)=c(A-) | |
| C. | a、b两点所示溶液中水的电离程度相同 | |
| D. | b点所示溶液中有 2c(Na+)=c(A-)+c(HA) |
10.配制0.5mol•L-1Na2CO3溶液100mL,下列操作导致溶液浓度偏高的是( )
| A. | 定容时俯视刻度线 | |
| B. | 容量瓶中原有少量蒸馏水 | |
| C. | 定容时液面高于刻度,用滴管小心吸去多余溶液,使液面与刻度相切 | |
| D. | 称取Na2CO3固体时,采用了“左码右物” |
7.下列事实不能用勒夏特列原理解释的是( )
| A. | 红棕色NO 2加压后颜色先变深后变浅 2NO2?N2O4 | |
| B. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| C. | SO2催化氧化成SO3的反应,使用过量的空气以提高二氧化硫的利用率 | |
| D. | H2、I2、HI平衡混合气体加压后颜色变深 |
3.已知:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0),往密闭容器中加入2molSO2、1milO2,下列说法正确的是( )
| A. | 充分反应后放出热量为Q | |
| B. | 增大压强,平衡右移,Q值变大 | |
| C. | 若生成1molSO3(s),放出热量大于$\frac{Q}{2}$ | |
| D. | 使用催化剂,改变反应途径,Q值也随之改变 |
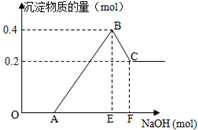 在HCl、MgCl2和AlCl3的混合溶液中,滴加NaOH溶液至过量,如图
在HCl、MgCl2和AlCl3的混合溶液中,滴加NaOH溶液至过量,如图 MgBr2
MgBr2