题目内容
4.有一组物质:①NaOH、②HCl、③MgBr2、④CO2、⑤白磷(P4)、⑥Na2O2、⑦H2O2、⑧N2、⑨NH4Cl、⑩CS2(1)请用序号填空:离子化合物有①③⑥⑨共价化合物有②④⑦⑩
(2)用电子式表示HCl和MgBr2的形成过程HCl
 MgBr2
MgBr2
(3)CS2的结构式:S=C=S.用极性键、非极性键、离子键填写:MgBr2含离子键键.NaOH含离子键和极性键键,Na2O2含离子键和非极性键键.
分析 (1)含有离子键的化合物属于离子化合物,只含有共价键的化合物属于共价化合物;
(2)HCl是共价化合物,分子中氢原子与氯原子之间形成1对共用电子对,用电子式表示其形成过程时,左边是原子的电子式,右边为HCl分子的电子式,中间用箭头连接;溴化镁是离子化合物,由钠离子与镁离子构成,用电子式表示其形成过程时,左边是原子的电子式,右边为溴化镁的电子式,中间用箭头连接;
(3)CS2是共价化合物,由极性键结合;溴化镁是离子化合物,由离子键结合;NaOH属于离子化合物,氢氧根离子中含有极性键;Na2O2属于离子化合物,过氧根离子中含有非极性键.
解答 解:(1)NaOH、MgBr2、Na2O2、NH4Cl均含有离子键,属于离子化合物;HCl、CO2、H2O2、CS2只含有共价键,属于共价化合物,P4、N2不属于化合物,
故答案为::①③⑥⑨;②④⑦⑩;
(2)HCl属于共价化合物,氢原子最外层电子与Cl最外层电子形成一对共用电子对,其形成过程可写为: ,
,
溴化镁是离子化合物,由钠离子与镁离子构成,用电子式表示的形成过程为 ,
,
故答案为: ;
; ;
;
(3)二硫化碳的结构式为S=C=S;溴化镁是离子化合物,由离子键结合;NaOH属于离子化合物,氢氧根离子中含有极性键;Na2O2属于离子化合物,含有离子键,过氧根离子中含有非极性键,
故答案为:S=C=S;离子键;离子键和极性键;离子键和非极性键.
点评 本题考查化学键、离子化合物和共价化合物的区分、用电子式的形成过程,题目难度不大,注意相关基础知识的积累.

| A. | 甲苯无同分异构体 | |
| B. | 邻二甲苯只有一种 | |
| C. | 苯分子中各原子均在一个平面内,各键键角均为120° | |
| D. | 1mol苯最多只能与3mol H2加成 |
| A. | 10-3 | B. | 10-7 | C. | 10-11 | D. | 10-14 |
 短周期元素X、Y、Z、W在元索周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子 数的三倍,下列说法不正确的是( )
短周期元素X、Y、Z、W在元索周期表中的相对位置如图所示,其中W原子的质子数是其最外层电子 数的三倍,下列说法不正确的是( )| A. | 原子半径:Z>W>X>Y | |
| B. | 最高价氧化物对应水化物的酸性:X>W>Z | |
| C. | 最简单气态氢化物的热稳定性:X>Y>Z>W | |
| D. | 元素X、Z、W的最高化合价分别与其主族序数相等 |
| A. | 将FeCl3溶液加热蒸干,可得到FeCl3固体 | |
| B. | 将PH=9的KOH溶液稀释1000倍后,其PH=6 | |
| C. | 用NaOH溶液滴定醋酸溶液时,不宜选用甲基橙作指示剂 | |
| D. | 碳酸溶液中氢离子浓度是碳酸根离子浓度的二倍 |
仅依据下表给出的物理量X和Y,其中不能求出物质的量的是
A | B | C | D | |
X | 物质中的粒子数 | 标准状况下的 气体摩尔体积 | 固体的体积 | 溶液中溶质的 物质的量浓度 |
Y | 阿伏加德罗常数 | 标准状况下 气体的体积 | 固体的密度 | 溶液体积 |
| 物质(杂质) | 试剂 | 方法 | |
| A | Cl2(HCl) | 饱和食盐水,浓硫酸 | 洗气 |
| B | 溴化钠(溴) | CCl4、水 | 萃取、分液 |
| C | 乙醇(乙酸) | NaOH溶液 | 分液 |
| D | 溴苯(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
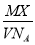 表示的是
表示的是 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示. 的
的