题目内容
3.已知:2SO2(g)+O2(g)?2SO3(g)+Q(Q>0),往密闭容器中加入2molSO2、1milO2,下列说法正确的是( )| A. | 充分反应后放出热量为Q | |
| B. | 增大压强,平衡右移,Q值变大 | |
| C. | 若生成1molSO3(s),放出热量大于$\frac{Q}{2}$ | |
| D. | 使用催化剂,改变反应途径,Q值也随之改变 |
分析 A.该反应为可逆反应,反应物不可能完全转化成生成物;
B.Q的值与化学计量数及物质状态有关,与压强大小无关;
C.三氧化硫固体具有的能量低,则放出的能量增大;
D.催化剂不影响化学平衡,则不影响反应热.
解答 解:A.往密闭容器中加入2molSO2、1milO2,由于该反应为可逆反应,则反应生成的三氧化硫的物质的量小于2mol,放出的热量小于Q,故A错误;
B.Q的数值与物质状态、化学计量数有关,所以增大压强,平衡右移,Q值不变,故B错误;
C.三氧化硫固体具有的能量小于三氧化硫气体,所以若生成1molSO3(s),放出热量大于$\frac{Q}{2}$,故C正确;
D.催化剂影响化学反应速率,但不影响化学平衡,所以使用催化剂后反应热不变,故D错误;
故选C.
点评 本题考查了化学平衡的计算,题目难度中等,明确可逆反应特点为解答关键,注意掌握化学平衡及其影响因素,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.能够说明苯分子中不存在单、双键,而是所有碳碳键完全相同的事实是( )
| A. | 甲苯无同分异构体 | |
| B. | 邻二甲苯只有一种 | |
| C. | 苯分子中各原子均在一个平面内,各键键角均为120° | |
| D. | 1mol苯最多只能与3mol H2加成 |
16.下列说法正确的是( )
| A. | 将FeCl3溶液加热蒸干,可得到FeCl3固体 | |
| B. | 将PH=9的KOH溶液稀释1000倍后,其PH=6 | |
| C. | 用NaOH溶液滴定醋酸溶液时,不宜选用甲基橙作指示剂 | |
| D. | 碳酸溶液中氢离子浓度是碳酸根离子浓度的二倍 |
仅依据下表给出的物理量X和Y,其中不能求出物质的量的是
A | B | C | D | |
X | 物质中的粒子数 | 标准状况下的 气体摩尔体积 | 固体的体积 | 溶液中溶质的 物质的量浓度 |
Y | 阿伏加德罗常数 | 标准状况下 气体的体积 | 固体的密度 | 溶液体积 |
14.下列关于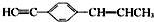 的说法正确的是( )
的说法正确的是( )
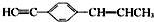 的说法正确的是( )
的说法正确的是( )| A. | 所有碳原子有可能都在同一个平面上 | |
| B. | 最多可能有9个碳原子在同一平面上 | |
| C. | 只能有4个碳原子在同一直线上 | |
| D. | 有7个碳原子可能在同一条直线上 |
11.某同学选择恰当的试剂和方法除去下列物质中少量杂质(括号内为杂质),下列各项中不正确的是( )
| 物质(杂质) | 试剂 | 方法 | |
| A | Cl2(HCl) | 饱和食盐水,浓硫酸 | 洗气 |
| B | 溴化钠(溴) | CCl4、水 | 萃取、分液 |
| C | 乙醇(乙酸) | NaOH溶液 | 分液 |
| D | 溴苯(溴) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
12.一般情况下,前者无法决定后者的是( )
| A. | 原子核外电子排布--元素在周期表中的位置 | |
| B. | 硝酸具有强氧化性--铜单质易溶于浓硝酸 | |
| C. | 分子间作用力的大小--分子稳定性的高低 | |
| D. | 二氧化硫具有还原性--二氧化硫能使高锰酸钾溶液褪色 |
 的
的