��Ŀ����
8��ij��ѧʵ��С���ͬѧΪ̽���ͱȽ�SO2����ˮ��Ư���ԣ���������µ�ʵ��װ�ã�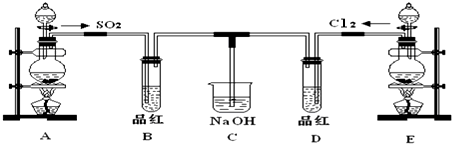
��1��ʵ������װ��A�Ʊ�SO2�����������SO2�������ԣ�����ԡ��������ԡ����ԡ��������
��2��ʵ������װ��E�Ʊ�Cl2��д���÷�Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2������Ӧ�е�Һ�巴Ӧ���ڷ�Ӧ�������ֳ�������Ϊ����ԭ�Ժ����ԣ�
��3����Ӧ��ʼһ��ʱ��۲쵽B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ�����ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�Ϊ
B����Һ����ɫ��Ϊ��ɫ��D������������
��4����һ��ʵ��С���ͬѧ��ΪSO2����ˮ����Ư���ԣ�����Ϻ��Ư���Կ϶����ǿ�����ǽ��Ƶõ�SO2��Cl2��1��1ͬʱͨ�뵽Ʒ����Һ�У����������ɫЧ��������������������������������ԭ���û�ѧ����ʽ��ʾ��SO2+Cl2+2H2O=H2SO4+2HCl��
��5��Cװ����β������װ�ã�д��Cװ�ô������������ӷ���ʽCl2+2OH-�TCl-+ClO-+H2O��
���� A�����Ʊ�SO2��ʵ�������������ƹ��������ᷴӦ��ȡSO2���壬�÷�ӦΪNa2SO3+H2SO4�TNa2SO4+SO2��+H2O��B���ڼ��������������ɣ�E��Ũ����Ͷ��������ڼ����������Ʊ�������D���ڼ��������Ư���ԣ�C��������β����
��1�������������ǺͼӦ�����κ�ˮ������������������Ǻ��ᷴӦ�����κ�ˮ����������ܺ��ᷴӦ���ܺͼӦ��������Ϊ���������
��2��ʵ������װ��E�Ʊ�Cl2��ΪMnO2��Ũ�����ڼ��ȵ��������Ʊ��������ݴ���д����ʽ�������ڸ÷�Ӧ�б��ֳ���ԭ�Ժ����ԣ�
��3�������Ͷ���������ʹƷ����Һ��ɫ�����Ƕ�������Ư������ʾ��в��ȶ��ԣ�����ʱ���ܱ�Ϊ��ɫ����������Ư���в������ԣ�
��4��SO2��Cl2��1��1ͨ�룬SO2��Cl2ǡ�÷�Ӧ�����߷�Ӧ����H2SO4��HCl�������ﶼ��Ư���ԣ�
��5���������������Ʒ�Ӧ�����Ȼ��ơ��������ƺ�ˮ��
��� �⣺��1�����������ܺͼӦ�����κ�ˮ���������������
�ʴ�Ϊ�����ԣ�
��2��ʵ������MnO2��Ũ�����ڼ��ȵ��������Ʊ���������Ӧ�ж�����������Ԫ�ش�+4�۽�Ϊ�Ȼ�����+2�ۣ������Ȼ�����-1�۵�������Ϊ������0�ۣ����ݵ�ʧ�����غ㣬���������ϵ��Ϊ1������ϵ��Ϊ1������ԭ�Ӹ����غ㣬��Ӧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2�����Ȼ����е���Ԫ����һ�뻯�ϼ����߱�����������Ϊ��ԭ�ԣ���һ�뻯�ϼ۲��䣬����Ϊ���ԣ�
�ʴ�Ϊ��MnO2+4HCl��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2H2O+Cl2������ԭ�Ժ����ԣ�
��3�������Ͷ���������ʹƷ����Һ��ɫ�����Ƕ�������Ư������ʾ��в��ȶ��ԣ�����ʱ���ܱ�Ϊ��ɫ����������Ư���в������ԣ������ٸ�B��D�����Թֱܷ���ȣ������Թ��е�����ֱ�ΪB����Һ����ɫ��Ϊ��ɫ��D������������
�ʴ�Ϊ����Һ����ɫ��Ϊ��ɫ������������
��4��SO2��Cl2��1��1ͨ�룬SO2��Cl2ǡ�÷�Ӧ�����߷�Ӧ����H2SO4��HCl�������ﶼ��Ư���ԣ�����ʽΪ��SO2+Cl2+2H2O=H2SO4+2HCl�������ﶼ��Ư���ԣ�
�ʴ�Ϊ��SO2+Cl2+2H2O=H2SO4+2HCl��
��5��������NaOH��Ӧ����NaCl��NaClO��ˮ��������ˮ�����ӷ�Ӧ�б�����ѧʽ�������ӷ�Ӧ����ʽ��Cl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
���� ���⿼�����ʵ�����ʵ�飬������ѧ���ķ�����ʵ�������Ŀ��飬��Ŀ�漰������������������ȡ�Լ���������Ư���������Ư��������Ŀ�Ѷ��еȣ�ע��β���Ĵ���������

| A�� | ����������Һ�еμ�ϡ����õ���pH=5�Ļ����Һ��c��Na+���Tc��NO3-�� | |
| B�� | 0.1mol/Lij��Ԫ����ǿ����NaHA��Һ�У�c��Na+���T2c��A2-��+c��HA-��+c��H2A�� | |
| C�� | 10mL0.5mol/L CH3COONa��Һ��6mL1mol/L������c��Cl-����c��Na+����c��OH-����c��H+�� | |
| D�� | �����£�0.1mol/L pH=4��NaHB��Һ�У�c��HB-����c��H2B����c��B2-�� |
| A�� |  ̫���������� | B�� |  ��̫���ܵ�� | C�� |  ȼ���� | D�� |  ����ӵ�� |
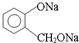 ת��Ϊ
ת��Ϊ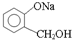 �����Լ��루������
�����Լ��루������| A�� | ˮ | B�� | ̼��������Һ | C�� | ̼�� | D�� | ���� |
| A�� | ��������ˮ�� | |
| B�� | �ڼ��������¶�����̼��Ӧ | |
| C�� | ¶���ڿ����ж����γɰ��� | |
| D�� | �ڿ����г���¶�ã���Һ���������� |
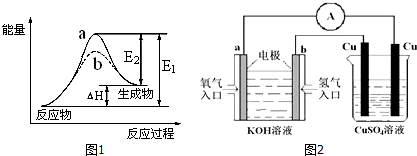
 ijͬѧ����ͼ��ʾװ��̽��SO2�����ʼ����й�ʵ�飮
ijͬѧ����ͼ��ʾװ��̽��SO2�����ʼ����й�ʵ�飮