题目内容
17.下列关于浓HNO3与浓H2SO4的叙述正确的是( )| A. | 都具有脱水性 | |
| B. | 在加热条件下都能与碳反应 | |
| C. | 露置于空气中都能形成白雾 | |
| D. | 在空气中长期露置,溶液质量均减轻 |
分析 A.浓硝酸不具有脱水性;
B.浓硝酸、浓硫酸都具有强的氧化性,加热条件下都能够氧化碳;
C.依据浓硝酸的挥发性和浓硫酸难挥发性解答;
D.依据浓硝酸的挥发性和浓硫酸吸水性解答.
解答 解:A.浓硝酸不具有脱水性,故A错误;
B.浓硝酸、浓硫酸在加热条件下都能与碳反应,故B正确;
C.浓硝酸具有挥发性,敞口放置挥发的硝酸与水蒸气生成白雾,浓硫酸难挥发,不会形成白雾,故C错误;
D.浓硝酸具有挥发性和浓硫酸吸水性,所以在空气中长期露置,溶液质量前者减少,后者增加,故D错误;
故选:B.
点评 本题考查了元素化合物知识,熟悉浓硫酸、浓硝酸的性质是解题关键,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
12.下列说法正确的是( )
| A. | 升高温度能使化学反应速率增大,主要原因是降低了反应活化能 | |
| B. | 有气体参加的化学反应,增大压强一定可以增大化学反应速率 | |
| C. | 增大反应物浓度,可提高单位体积内活化分子的百分数,从而使有效碰撞次数增大 | |
| D. | 催化剂的加入能提高单位体积内活化分子百分数,从而增大化学反应速率 |
9.下列现象或事实能用同一原理解释的是( )
| A. | 水玻璃和硫酸亚铁溶液长期暴露在空气中均易变质 | |
| B. | SO2和CO2通入CaCl2溶液中均无明显现象 | |
| C. | 浓硫酸和浓盐酸长期暴露在空气中浓度降低 | |
| D. | SO2、漂白粉、活性炭都能使红墨水褪色 |
6.在下列给定条件的溶液中,一定能大量共存的离子组是( )
| A. | 无色溶液:Cu2+、H+、Cl-、HSO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、Fe2+、Cl-、NO3- | |
| C. | 在水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Fe3+、Cl-、NO3- | |
| D. | $\frac{{K}_{w}}{c({H}^{+})}$=0.1 mol/L的溶液:Na+、K+、SiO32-、NO3- |
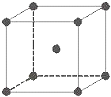 金属铁晶体为体心立方堆积(如图),实验测得铁的密度为ρ(g•cm-3).已知铁的相对原子质量为a,阿伏加德罗常数为NA(mol-1).
金属铁晶体为体心立方堆积(如图),实验测得铁的密度为ρ(g•cm-3).已知铁的相对原子质量为a,阿伏加德罗常数为NA(mol-1).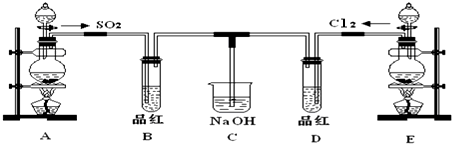
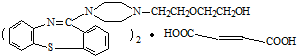 ,它的合成路线如下:
,它的合成路线如下: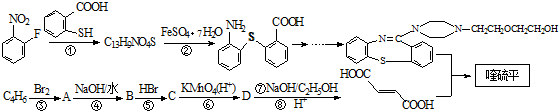
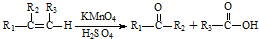
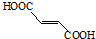 含有的官能团名称为碳碳双键和羧基.
含有的官能团名称为碳碳双键和羧基.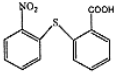 .
.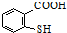 在一定条件下发生缩聚反应的化学方程式为
在一定条件下发生缩聚反应的化学方程式为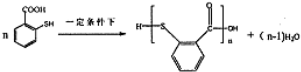 .
.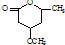 是一种重要的有机化合物.请设计合理方案,完成从
是一种重要的有机化合物.请设计合理方案,完成从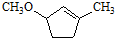 到
到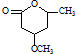 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).