题目内容
19.“8•12”天津港危化仓库爆炸,造成生命、财产的特大损失.据查危化仓库中存有大量的钠、钾,硝酸铵和氰化钠(NaCN).请回答下列问题:(1)钠、钾着火,下列可用来灭火的是D(填字母).
A.水 B.泡沫灭火器 C.干粉灭火器 D.细沙盖灭
(2)NaCN是属于离子化合物(填“离子化合物”或“共价化合物”),NaCN的电子式为:Na+
 .
.(3)白磷有毒,能和氯酸溶液发生氧化还原反应:3P4+10HClO3+18H2O═10HCl+12H3PO4,该反应的氧化剂是HClO3,氧化产物是H3PO4,若有1mol P4参加反应转移电子为20mol.
(4)NH4NO3为爆炸物,在不同温度下加热分解,可能发生非氧化还原反应,可能发生氧化还原反应,请写出发生非氧化还原反应的热分解方程式NH4NO3=NH3↑+HNO3.
(5)NaCN属于剧毒物质,有多种无害化处理方法,H2O2处理法是其中之一:NaCN+H2O2→N2↑+X+H2O,推测X的化学式为NaHCO3.
分析 (1)Na、K均与水反应,燃烧生成的过氧化氢均与二氧化碳反应生成氧气;
(2)NaCN为离子化合物;
(3)该反应中,P元素化合价由0价变为+5价、Cl元素化合价由+5价变为-1价,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物;
若有1mol P4参加反应转移电子物质的量=1mol×4×(5-0);
(4)NH4NO3分解,一种可能是发生复分解反应,还有一种可能是氧化还原反应,根据氧化还原反应中有元素化合价升高就必须有元素化合价降低的原则进行书写;
(5)根据元素守恒确定X中元素,根据转移电子守恒、原子守恒确定X化学式.
解答 解:(1)Na、K均与水反应,燃烧生成的过氧化氢均与二氧化碳反应生成氧气,则钠、钾着火,可用细沙盖灭来灭火,故答案为:D;
(2)NaCN为离子化合物,电子式为Na+ ,故答案为:离子化合物;Na+
,故答案为:离子化合物;Na+ ;
;
(3)该反应中,P元素化合价由0价变为+5价、Cl元素化合价由+5价变为-1价,得电子化合价降低的反应物是氧化剂,失电子化合价升高的反应物是还原剂,还原剂对应的产物是氧化产物,所以HClO3是氧化剂、H3PO4是氧化产物;
若有1mol P4参加反应转移电子物质的量=1mol×4×(5-0)=20mol;
故答案为:HClO3; H3PO4;20;
(4)NH4NO3=NH3↑+HNO3为分解反应,但元素化合价没有发生变化,不是英汉互译反应,故答案为:NH4NO3=NH3↑+HNO3;
(5)根据元素守恒知,X中含有Na、C元素,该反应中N元素化合价由-3价转化为0价、NaCN中C元素化合价为+2价,则C元素化合价由+2价转化为+4价,转移电子数为6,根据转移电子守恒、原子守恒知X为NaHCO3,
故答案为:NaHCO3
点评 本题考查氧化还原反应的计算及含量测定等,综合性较强,注重高频考点的考查,侧重分析与计算能力的考查,注意反应中元素的化合价变化,题目难度中等.

| A. | 苯与浓硝酸、浓硫酸共热并保持55-60℃反应生成硝基苯 | |
| B. | 苯不能使酸性高锰酸钾褪色,说明苯环中没有碳碳双键 | |
| C. | 甲烷中混有的乙烯可以用溴的四氯化碳溶液除去 | |
| D. | 医院用75%酒精杀菌、消毒,75%是指质量分数 |
| A. | 甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 | |
| B. | 有机物  的消去(分子内脱水)产物只有2种 的消去(分子内脱水)产物只有2种 | |
| C. | 有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是CH2═CH-COOCH3 | |
| D. | 可用溴水鉴别已烯、四氯化碳和乙酸 |
| A. | 6 | B. | 9 | C. | 12 | D. | 18 |
| A. | 1×10-5mol/L | B. | 1×10-12mol/L | C. | 1×10-6mol/L | D. | 1×10-7mol/L |
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配 料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
1IO3-+5I-+6H+=3I2+3H2O
(2)上述反应生成的I2可用四氯化碳检验.向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳.
①Na2SO3稀溶液与I2反应的离子方程式是I2+SO32-+H2O=2I-+SO42-+2H+.
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;b.加入适量Na2SO3稀溶液;c.分离出下层液体.
以上设计中遗漏的操作及在上述步骤中的位是在步骤b后,增加操作;
所缺步骤为将分液漏斗充分振荡后静置
(3)已知:I2+2S2O32-=2I-+S4O62-.某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为6.0×10-4mol•L-1的Na2S2O3溶液20.0mL,恰好反应完全.
①判断c中反应恰好完全依据的现象是滴入最后一滴溶液时,溶液的蓝色恰好消失,且半分钟内不恢复原色,则达到滴定终点.
②根据以上实验和包装袋说明,所测精制盐的碘含量是20 mg/kg.
| A. | 含有食品添加剂的物质均对人体健康有害 | |
| B. | 磨豆浆的大豆富含蛋白质,豆浆煮沸后蛋白质变成了氨基酸 | |
| C. | 现代海战通过喷放液体SiCl4(极易水解)和液氨可产生烟幕,其主要成分是NH4Cl | |
| D. | 明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
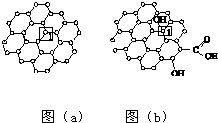 石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].
石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示].