题目内容
下列关于能量变化的说法正确的是( )
| A、相同质量的水和冰相比较,冰的能量高 |
| B、化学反应过程中能量的变化只有吸热和放热两种表现形式 |
| C、化学反应既遵循质量守恒,也遵循能量守恒 |
| D、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、H2O(l)=H2O(s)△H<0,液态水到固态水,放热,所以水的能量高;
B、化学反应还伴随着能量变化,通常表现为反应过程中的放热或吸热;
C、化学反应遵循质量守恒的同时,也遵循能量守恒;
D、石墨完全转化为金刚石时,要吸收能量,说明金刚石能量高于石墨,能量越低越稳定.
B、化学反应还伴随着能量变化,通常表现为反应过程中的放热或吸热;
C、化学反应遵循质量守恒的同时,也遵循能量守恒;
D、石墨完全转化为金刚石时,要吸收能量,说明金刚石能量高于石墨,能量越低越稳定.
解答:
解:A、H2O(l)=H2O(s)△H<0,液态水到固态水,放热,所以水的能量高,故A错误;
B、化学反应还伴随着能量变化,通常表现为反应过程中的放热或吸热,也可以表现为其他形式的能量,故B错误;
C、化学反应遵循质量守恒的同时,也遵循能量守恒,故C正确;
D、石墨完全转化为金刚石时,要吸收能量,说明金刚石能量高于石墨,能量越低越稳定,所以石墨比金刚石稳定,故D错误;
故选C.
B、化学反应还伴随着能量变化,通常表现为反应过程中的放热或吸热,也可以表现为其他形式的能量,故B错误;
C、化学反应遵循质量守恒的同时,也遵循能量守恒,故C正确;
D、石墨完全转化为金刚石时,要吸收能量,说明金刚石能量高于石墨,能量越低越稳定,所以石墨比金刚石稳定,故D错误;
故选C.
点评:本题考查了物质能量的高低与反应能量变化的关系、能量转化的形式等问题,难度不大,根据所学知识即可完成.

练习册系列答案
相关题目
下列实验中,操作正确且能达到相应实验目的是( )
| A、做中和热测定实验时,若没有环形玻璃搅拌棒,可用环形铜质搅拌棒代替 |
| B、中和滴定实验中,左手调控滴定管的活塞,右手持锥形瓶,眼睛注视滴定管中液面的变化 |
| C、溴蒸汽和二氧化氮两种红棕色气体可用淀粉碘化钾溶液来鉴别 |
| D、除去蛋白质溶液中少量的NaCl,可将装有混合液的半透膜袋浸入流动的蒸馏水中 |
以下对化学实验的描述合理的是( )
| A、配制一定物质的量浓度的硫酸溶液时,应将量取好的浓硫酸先放入烧杯中,然后加水稀释 |
| B、中和滴定实验前,所使用的滴定管和锥形瓶必须洗净,并用待测液润洗 |
| C、测定Na2CO3、Na2SO4两溶液的pH,比较碳、硫的非金属性强弱 |
| D、硫酸铜晶体结晶水含量的测定实验中,盛晶体的坩埚灼烧后,需放在石棉网上冷却后称量 |
如图是某水溶液在pH从 0至14的范围内,H2CO3、HCO3-、CO32-三种粒子平衡时的组成百分率,下列叙述不正确的是( )
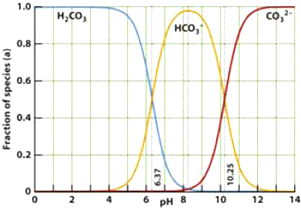

| A、此图可完全根据1.0 mol/L盐酸滴定1.0 mol/L碳酸钠溶液的实验数据绘出 |
| B、H2CO3和CO32-在溶液中不能大量共存 |
| C、将1.0 mol/L盐酸加入到等体积1.0 mol/L碳酸钠溶液中,充分反应后溶液呈碱性 |
| D、在pH为6.37时,溶液中:c(H2CO3)=c(HCO3-),在pH为10.25时,溶液中:c(CO32-)=c(HCO3-) |
CaCO3与稀盐酸反应(放热反应)生成CO2的量与反应时间的关系如图所示.下列结论不正确的是( )


| A、反应开始4 min内温度对反应速率的影响比浓度大 |
| B、一段时间后,反应速率减小的原因是c(H+)减小 |
| C、反应在2~4 min内平均反应速率最大 |
| D、反应在2~4 min内生成CO2的平均反应速率为V(CO2)=0.1 mol?L-1?min-1 |
稀氨水中存在着下列平衡:NH3?H2O═NH4++OH-,若要使平衡向左移动,同时使c(OH-)增大,应加入适量的物质是( )
| A、NH4Cl |
| B、H2SO4 |
| C、NaOH |
| D、H2O |
下列说法正确的是( )
| A、糖类、油脂和蛋白质是基本营养物质,它们都是天然高分子化合物 |
| B、蛋白质水解的最终产物是多肽 |
| C、米酒变酸的过程涉及了氧化反应 |
| D、向蛋白质溶液中加入浓的Na2SO4溶液可使蛋白质盐析而分离提纯 |
对于可逆反应:2SO2+O2
2SO3+Q,下列措施能使反应物中活化分子百分数、化学反应速率和化学平衡常数都变化的是( )
| 催化剂 |
| A、增大压强 |
| B、升高温度 |
| C、使用催化剂 |
| D、多充入O2 |

 )是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖.
)是味精的主要成分.当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖.