题目内容
19.下列操作中正确的是( )| A. | 向试管中滴加液体时,胶头滴管紧贴试管内壁 | |
| B. | 浓硫酸沾在皮肤上时应用大量水冲洗,再涂上3%~5%的NaOH溶液 | |
| C. | 实验室进行蒸馏操作时若忘加了沸石,应停止反应冷却至室温后再加入 | |
| D. | 配制硫酸溶液时,可先在量筒中加一定体积的水,再在搅拌条件下慢慢加入浓硫酸 |
分析 A.向试管内滴加液体时胶头滴管应竖直悬空;
B.NaOH具有强腐蚀性;
C.立即加入沸石会引起爆沸;
D.浓硫酸稀释时应该在烧杯中进行.
解答 解:A.向试管内滴加液体时胶头滴管应竖直悬空,不能紧贴试管内壁,否则易导致胶头滴管产生杂质,故A错误;
B.NaOH具有强腐蚀性,能腐蚀皮肤,碳酸氢钠具有弱碱性,能中和硫酸且腐蚀性较小,所以应该用碳酸氢钠涂抹,故B错误;
C.即加入沸石会引起爆沸,应冷却后再加入,故C正确;
D.浓硫酸稀释时应该在烧杯中进行,量筒只能量取液体,不能溶解或稀释药品,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及实验基本操作、仪器用途、实验安全等知识点,明确实验原理、实验操作规范性、仪器用途是解本题关键,侧重考查学生实验操作、实验评价能力,题目难度不大.

练习册系列答案
相关题目
9.核外电子数相等的原子一定是( )
①同种元素 ②同种原子 ③质子数相同 ④质量数相同 ⑤互为同位素.
①同种元素 ②同种原子 ③质子数相同 ④质量数相同 ⑤互为同位素.
| A. | ①②③ | B. | ①③⑤ | C. | ①②③④ | D. | 全部 |
10.已知四价铅有强氧化性,能跟盐酸反应生成氯气,将SO2通入悬浮着黑色PbO2的热水中,过一会儿,将发生的情形是( )
| A. | 悬浮物由黑色变为白色,因SO2是一种漂白剂 | |
| B. | 悬浮物由黑色变为白色,因为形成了PbSO4 | |
| C. | 有黄色沉淀生成 | |
| D. | 有臭鸡蛋味的气体放出 |
7.某有机物R的结构简式如图所示.下列关于R的说法不正确的是( )
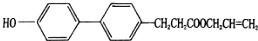

| A. | 能发生加成、加聚、水解和氧化反应 | |
| B. | 分子式为C18H20O3 | |
| C. | 该化合物最多有12个碳原子共平面 | |
| D. | 一定条件下1molR最多可以消耗2molNaoH |
4.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | c(H+)=$\sqrt{{K}_{W}}$mol•L-1的溶液:Fe3+、K+、Cl-、CO32- | |
| B. | c(NH4+)=0.1mol•L-1的(NH4)2Fe(SO4)2溶液:H+、Al3+、Br-、I- | |
| C. | 加水稀释时,$\frac{c(O{H}^{-})}{c({H}^{+})}$值明显增大的溶液:K+、NH4+、CO32-、MnO4- | |
| D. | 通入SO2的饱和溶液:Ca2+、K+、NO3-、Cl- |
9.已知:2H2(g)+O2(g)═2H2O(g)1molH2完全燃烧放出热量为241.8KJ有关键能数据如表:
则H-H键键能为( )
| 化学键 | H-O | O=O |
| 键能/KJ?mol-1 | 463.4 | 498 |
| A. | 413KJ/mol | B. | 872KJ/mol | C. | 221.6KJ/mol | D. | 436KJ/mol |