题目内容
7.能证明氯化钠的是离子化合物的实验事实是( )| A. | .氯化钠的水溶液能够导电 | B. | .氯化钠晶体中只存在离子键 | ||
| C. | .熔融的氯化钠可以导电 | D. | 氯化钠的熔沸点比较高 |
分析 说明氯化钠是离子化合物,只要证明氯化钠是由阴阳离子构成的即可,可溶性离子化合物在水溶液中或熔融状态下能导电,据此分析解答.
解答 解:A.氯化钠的水溶液能导电,说明氯化钠在水溶液中能发生电离,但不能说明氯化钠中含有阴阳离子,共价化合物的水溶液也可能得到,如硫酸等,故A错误;
B.离子化合物阴阳离子之间通过离子键结合,氯化钠晶体中只存在离子键,说明氯化钠的是离子化合物,故B正确;
C.熔融状态下氯化钠能导电,说明氯化钠中含有阴阳离子,所以为离子化合物,故C正确;
D.氯化钠的熔沸点比较高不能说明氯化钠是离子化合物,有些共价化合物的熔沸点比较高,如二氧化硅等,故D错误;
故选BC.
点评 本题考查离子化合物的判断,为高频考点,化合物类型与其构成微粒有关,与物质的水溶性、熔沸点等性质无关,题目难度不大.

练习册系列答案
相关题目
17.钢笔的笔头是合金钢,钢笔尖端是用机器轧出的便于使用的圆珠体.铱金笔的笔头是用不锈钢制成的,为了改变钢笔头的耐磨性能,在笔头尖端点上安装铱金粒,为与钢笔区别而叫铱金笔.金笔是笔头用黄金的合金,笔尖用铱的合金制成的高级自来水笔.下列说法中错误的是( )
| A. | 钢笔的笔头不易被氧化,抗腐蚀性能好 | |
| B. | 铱金笔的耐磨性能比钢笔好 | |
| C. | 金笔的笔头和笔尖都是用纯金制成的 | |
| D. | 金笔经久耐磨,是一种很理想的硬笔 |
18.反应2X+3Y═2Z消耗X的质量与生成Z的质量关系如图所示,下列说法正确的是( )
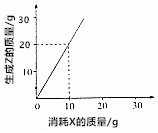

| A. | 有4g Z生成时,则消耗Y 3g | B. | X、Y、Z的摩尔质量之比为1:1:2 | ||
| C. | X、Y、Z的摩尔质量之比为2:3:2 | D. | X、Y、Z的摩尔质量之比为3:2:6 |
2.配制一定物质的量浓度的溶液,造成浓度偏高的操作是( )
| A. | 洗涤后的容量瓶未干燥 | B. | 移液后,未洗涤烧杯和玻璃棒 | ||
| C. | 定容时,眼睛视线俯视刻度线 | D. | 移液时,不慎将液体流到瓶外 |
12.化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A. | 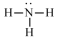 氨分子的结构式 | B. | 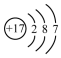 Cl-结构示意图 | C. | 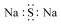 Na2S的电子式 | D. | 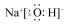 NaOH的电子式 |
19.下列各组中的离子,能在溶液中大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、Ca2+、CO32-、NO3- | ||
| C. | Na+、H+、CO32-、Cl- | D. | Na+、Cu2+、Cl-、SO42- |
16.下列气体中是非电解质,且和SO2一起通入到BaCl2溶液中可生成BaSO3沉淀的是( )
| A. | Cl2 | B. | H2S | C. | NH3 | D. | HCl |
17.同温同压下,A容器中的H2和B容器中的NH3所含氢原子数为3:2,则两个容器的体积比是( )
| A. | 3:2 | B. | 1:1 | C. | 9:4 | D. | 1:2 |
 的化合物与 CH2=CH2 一样,在一定条件下可聚合成高分子化合物.广泛用作 农用薄膜的聚氯乙烯塑料,是由 CH2=CH-Cl 聚合而成的,其化学反应方程式是
的化合物与 CH2=CH2 一样,在一定条件下可聚合成高分子化合物.广泛用作 农用薄膜的聚氯乙烯塑料,是由 CH2=CH-Cl 聚合而成的,其化学反应方程式是 .
.