题目内容
2.标准状况下,密度为0.75g/L的C2H4与CH4组成的混合气体中,C2H4的体积分数约为6.67%.(保留三位有效数字)分析 依据M=ρVm计算混合气体的平均摩尔质量,设物质的量之比为x:y,依据M=M1×ω1+M2ω2解答.
解答 解:标准状况下,密度为0.75g/L的C2H4与CH4组成的混合气体,M=0.75g/L×22.4L/mol=16.8g/mol,设C2H4的体积分数为x,则CH4体积分数为(1-x),依据平均摩尔质量计算公式可知:M=28x+16×(1-x)=16.8,解得x=6.67%;
故答案为:6.67%.
点评 本题考查了物质的量有关计算,明确平均摩尔质量计算公式是解题关键,题目难度不大,注意标况下M=ρVm,题目难度不大.

练习册系列答案
相关题目
13.随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
(l)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g) $\stackrel{RU}{?}$CH4(g)+2H2O(g)
已知CO2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列各物理量的变化.(选填“增大”、“减小”或“不变”)
v正增大,v逆增大,平衡常数K减小,转化率α减小.
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
a、b、c、d与m、n、x、y之间的关系式为$\frac{c{d}^{2}}{a{b}^{4}}$=$\frac{x{y}^{2}}{m{n}^{4}}$.
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变
(4)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2 4KO2+4CO2+2H2O→4KHCO3+3O2
若9molCO2在密封舱内和KO2反应后生成9molO2,则反应前密封舱内H20的量应该是3mol.
(l)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g) $\stackrel{RU}{?}$CH4(g)+2H2O(g)
已知CO2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列各物理量的变化.(选填“增大”、“减小”或“不变”)
v正增大,v逆增大,平衡常数K减小,转化率α减小.
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如表:
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
(3)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变
(4)CO2和KO2有下列反应:4KO2+2CO2→2K2CO3+3O2 4KO2+4CO2+2H2O→4KHCO3+3O2
若9molCO2在密封舱内和KO2反应后生成9molO2,则反应前密封舱内H20的量应该是3mol.
10. 中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
 中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )
中国是中草药的发源地,目前中国大约有12000种药用植物,从某中草药提取的有机物结构如图所示,该有机物的下列说法中不正确的是( )| A. | 分子式为C14H18O6 | |
| B. | 环上氢原子的一氯取代物5种 | |
| C. | 1mol该有机物与足量的金属钠反应产生4mol H2 | |
| D. | 分子间能发生酯化反应 |
17.下列关于物质的浓度的说法正确的是( )
| A. | 将5.85 g NaCl固体溶于1 L水中可配成0.1mol/L的NaCl 溶液 | |
| B. | 500 ml 0.5mol/L 的NaOH溶液含NaOH分子0.25 mol | |
| C. | 把200mL 3mol/L的BaCl2溶液跟100mL 3mol/L的KCl溶液混合后,溶液中的c(Cl-)仍然是3mol/L(忽略混合后体积变化) | |
| D. | 把100g 20%的NaCl溶液跟100g H2O混合后,NaCl溶液的质量分数是10% |
14.某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)?2C(g),达到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中物质的物质的量浓度、反应速率分别随时间的变化如图所示:下列说法中正确的是( )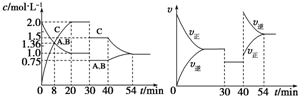

| A. | 30~40 min 间该反应使用了催化剂 | |
| B. | 反应方程式中的x=1,正反应为吸热反应 | |
| C. | 30 min 时降低温度,40 min 时升高温度 | |
| D. | 30 min时减小压强,40 min时升高温度 |
12.己知反应2FeCl3+Cu=CuCl2+2FeCl2,则下列判断正确的是( )
| A. | 该反应是置换反应 | B. | 该反应中FeCl3作还原剂 | ||
| C. | 还原性:Cu>Fe2+ | D. | 氧化性:CuCl2>FeCl3 |