题目内容
9.下列物质中既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )| A. | Al(OH)3 | B. | NaCl溶液 | C. | K2SO4溶液 | D. | 稀H2SO4 |
分析 Al、Al2O3、Al(OH)3、弱酸酸式盐、弱酸的铵盐、蛋白质、氨基酸等物质都能和稀盐酸、氢氧化钠溶液反应,据此分析解答.
解答 解:A.氢氧化铝是两性氢氧化物,能和稀盐酸、NaOH溶液反应生成盐和水,故A正确;
B.NaCl是强酸强碱盐,该物质不能和稀盐酸、NaOH反应,故B错误;
C.硫酸钾是强酸强碱盐,不能和稀盐酸、NaOH反应,故C错误;
D.稀硫酸具有酸性,能和NaOH反应生成盐和水,和稀盐酸不反应,故D错误;
故选A.
点评 本题考查元素化合物性质,为高频考点,明确物质性质及基本概念是解本题关键,注意基础知识的总结归纳,题目难度不大.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
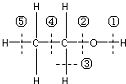
10.对于原子核外电子以及电子的运动,下列描述正确的是( )
①能量低的电子只能在s能级上运动,能量高的电子总是在f能级上运动
②电子质量很小且带负电荷
③运动的空间范围很小
④高速运动
⑤有固定的运动轨道
⑥电子的质量约为氢离子质量的$\frac{1}{1836}$.
①能量低的电子只能在s能级上运动,能量高的电子总是在f能级上运动
②电子质量很小且带负电荷
③运动的空间范围很小
④高速运动
⑤有固定的运动轨道
⑥电子的质量约为氢离子质量的$\frac{1}{1836}$.
| A. | ①②③ | B. | ②③④⑥ | C. | ③④⑤⑥ | D. | ⑤⑥ |
11.常温下,下列有关电解质溶液的说法正确的是( )
| A. | 0.1 mol•L-1Na2CO3溶液:c(Na+)>c(CO${\;}_{3}^{2-}$)>c(HCO${\;}_{3}^{-}$)>c(OH-) | |
| B. | 0.01 mol•L-1CH3COOH溶液,水电离出的c(H+)=10-12mol•L-1 | |
| C. | 0.2 mol•L-1NaClO溶液:c(Na+)═c(ClO-)+c(Cl-)+c(HClO) | |
| D. | pH相同的NH4Cl、(NH4)2SO4溶液:c(NH4Cl)>c[(NH4)2SO4] |
4.起固氮作用的化学反应的是( )
| A. | 雷电使氮气和氧气反应生成了一氧化氮气体 | |
| B. | 一氧化氮与氧气反应生成二氧化氮 | |
| C. | 氨气经催化氧化生成一氧化氮 | |
| D. | 由氨气制碳酸氢氨和硫酸氨 |
14.石油价格的波动直接影响着第三世界经济发展.下列关于石油的说法正确的是( )
| A. | 石油属于可再生矿物能源 | B. | 石油主要含有碳、氢两种元素 | ||
| C. | 石油的裂化是物理变化 | D. | 石油分馏的各馏分均是纯净物 |
18.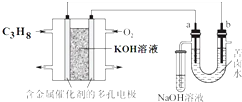 用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
 用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )
用碱性丙烷燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a、b为石墨电极),下列说法正确的是( )| A. | 电池工作时,负极反应式为:C3H8+26OH--20e-═3CO${\;}_{3}^{2-}$+17H2O | |
| B. | 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 | |
| C. | 电解时,电子流动的路径是:负极→外电路→阴极→溶液→阳极→正极 | |
| D. | 忽略能量损耗,当电池中消耗 0.16 g O2时,a极周围会产生0.71 g Cl2 |
19.在两个容积相同的容器中,一个盛有NH3气体,另一个盛有Cl2和H2的混合气体.在相同的温度和压强下,两容器内的气体一定具有相同的是( )
| A. | 质量 | B. | 密度 | C. | 原子数 | D. | 物质的量 |