题目内容
17.反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题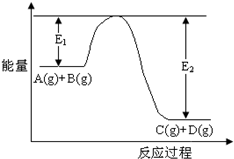
(1)该反应是放热反应(填“吸热”“放热”);
(2)反应体系中加入催化剂对反应热是否有影响?不影响,
(3)在反应体系中加入催化剂,反应速率增大,E1的变化是:E1减小,(填“增大”“减小”“不变”)
分析 (1)根据反应物总能量和生成物总能量的关系判断反应热;
(2)催化剂对平衡无影响;
(3)加入催化剂能降低物质的活化能.
解答 解:(1)由图象可以看出反应物总能量大于生成物的总能量,则该反应的正反应为放热反应,故答案为:放热;
(2)催化剂能加快反应速率但不改变平衡的移动,所以反应热不变,故答案为:不影响;
(3)加入催化剂能降低反应物质的活化能,则E1和E2都减小,故答案为:减小.
点评 本题考查反应热的判断,影响化学反应速率的因素,题目难度不大,掌握基础是解题关键.

练习册系列答案
相关题目
5.《汉书》记载“高奴(县)有洧水可燃”;《梦溪笔谈》描述“洧水”:“予知其烟可用,试扫其烟为墨,黑光如漆,松墨不及也,此物必大行于世”.上述有关“洧水”和“烟”的主要成分分别是( )
| A. | 石油和炭黑 | B. | 石油和焦炭 | C. | 油脂和木炭 | D. | 油脂和石墨 |
12.某学生的实验操作中合理的是( )
| A. | 用10mL量筒量取7.13mL稀盐酸 | |
| B. | 用碱式滴定管量取15.20 ml 酸性高锰酸钾溶液 | |
| C. | 配制氯化铁溶液时,把氯化铁溶解在一定浓度的盐酸中,再加水稀释 | |
| D. | 用带有橡胶塞的玻璃试剂瓶盛放NaF溶液 |
9.下列物质中既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A. | Al(OH)3 | B. | NaCl溶液 | C. | K2SO4溶液 | D. | 稀H2SO4 |
6.下列说法不正确的是( )
| A. | 生物酶固氮相比人工固氮更高效、条件更温和 | |
| B. | 透过观察颜色容易区分黄金与铜锌合金 | |
| C. | 近日用地沟油炼制的生物航油载客首飞,标志着我国航空业在节能减排领域进入商业飞行阶段 | |
| D. | 尿液燃料电池的原理是在微生物作用下将尿液中的有机物转化为电能 |
7.下列说法正确的是( )
| A. | 聚乙烯固定的熔沸点,其可由乙烯通过加聚反应合成 | |
| B. | 有机物的种类繁多,分子中含有碳、氢元素的物质即为有机物 | |
| C. | 石油的分馏和煤的干馏均属于物理变化 | |
| D. | 不是所有的有机物中都含有一种或多种官能团 |