题目内容
某小组为研究电化学原理,设计如图装置。下列叙述错误的是
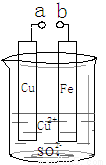
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e-= Cu
C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动
D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色
C
【解析】
试题分析:A.a和b不连接时,铁与硫酸铜发生置换反应生成铜与硫酸亚铁。生成的铜附着在铁片上,正确;B.a和b用导线连接时构成原电池,铁的金属性强于铜,因此铁是负极,铜是正极,则正极发生的电极反应为:Cu2++2e-=Cu,正确;C.a和b分别连接电源正、负极时,构成电解池。Fe电极是阴极,Cu2+向铁电极移动,错误;D.a和b用导线连接时构成原电池,铁的金属性强于铜,因此铁是负极失去电子而被腐蚀。a和b不连接时,铁与硫酸铜发生置换反应生成铜与硫酸亚铁而被腐蚀,正确;选C。
考点:考查电化学原理的有关应用与判断。

练习册系列答案
相关题目

 N2O4(g),在相同条件下,若分别向容器中通入一定量的NO2气体或N2O4气体,重新达到平衡后,容器内N2O4的体积分数比原平衡时
N2O4(g),在相同条件下,若分别向容器中通入一定量的NO2气体或N2O4气体,重新达到平衡后,容器内N2O4的体积分数比原平衡时