题目内容
关于下列各装置图的叙述中,不正确的是

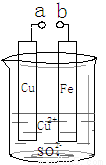
A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+
C.装置③中钢闸门应与外接电源的负极相连
D.装置④中的铁钉几乎没被腐蚀
B
【解析】
试题分析:A.Cu精炼时粗铜作阳极,精铜作阴极,含有Cu2+的溶液作电解液,电流流入的电极a为阳极,正确;B. 由于活动性Fe>Cu,所以在装置②的原电池反应中,Fe作负极,Cu作正极,总反应是:Fe+2Fe3+=3Fe2+,错误;C. 装置③中钢闸门与外接电源的负极相连,做阴极,得到保护,正确; D.因为Fe在常温下干燥的环境中几乎不被腐蚀,浓硫酸具有吸水性,所以在装置④中的铁钉由于钝化几乎没被腐蚀,正确;选B。
考点:考查金属的腐蚀与防护,电解等知识。

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
 后的某一时刻后,加压,平衡左移,造成这一结果的原因可能是
后的某一时刻后,加压,平衡左移,造成这一结果的原因可能是 
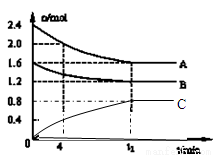
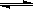 C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。
C(g)+D(g),最初加入1.0molA和2.2molB,在不同温度下,D的物质的量n(D)和时间t的关系如图。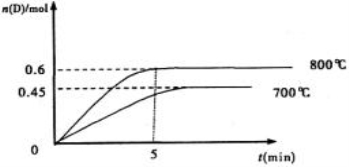
 CH3COO-+H+ 对于该平衡,下列叙述正确的是
CH3COO-+H+ 对于该平衡,下列叙述正确的是