题目内容
下列性质中,可以证明某化合物内一定存在离子键的是
A.可溶于水 B.具有较高的熔点
C.水溶液能导电 D.熔融状态能导电
D
【解析】
试题分析:某化合物内一定存在离子键,则该化合物一定是离子化合物,构成微粒为阴阳离子,熔融状态下能电离出自由移动的阴阳离子,能导电,故D项正确;一些共价化合物也可溶于水,水溶液能导电,例如HCl,某些共价化合物也有较高的熔点,例如SiO2,故A、B、C均错误。
考点:离子化合物。

练习册系列答案
相关题目
下列离子方程式正确的是
A.用CH3COOH溶解CaCO3: CaCO3+2H+=Ca2++H2O+C02↑ |
B.Fe2(SO4)3和Ba(OH) 2溶液混合:Fe3++SO42-+Ba2++3OH-Fe(OH)3↓+ BaSO4↓ |
C.硫酸工业尾气中的SO2用过量的氨水吸收:2NH3·H2O+ SO2 =2NH4++ SO32-+H2O |
D.Cu溶于浓HNO3:Cu+ 4H++ 2NO3一=Cu2++ 2NO↑+ 4H2O |
 MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。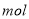 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________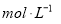 。
。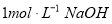 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。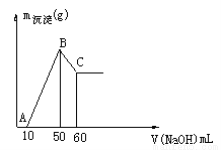
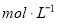 。
。