题目内容
有关常温下pH均为3的醋酸和硫酸的说法正确的是
A.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol/L
B.分别加水稀释100倍后,两种溶液的pH仍相同
C.醋酸中的c(CH3COO-)和硫酸中的c(SO42-)相等
D.分别加入足量锌片,两种溶液生成H2的体积相同
A
【解析】
试题分析:A、两溶液中氢离子浓度为10-3 mol/L,根据水的离子积常数计算,氢氧根离子浓度为10-11 mol/L,溶液中水电离出的氢离子浓度等于溶液中的氢氧根离子浓度,故两种溶液中水电离的氢离子浓度为1×10-11 mol/L ,选A;B、硫酸是强电解质,完全电离,加水稀释后pH为5,醋酸是弱电解质,加水稀释后,电离平衡正向移动,继续电离出氢离子,所以pH小于5,故不选B;C、由电荷可知,醋酸中醋酸根离子浓度等于氢离子浓度,为10-3 mol/L ,硫酸根离子浓度为氢离子浓度的一半,故不选C;D、硫酸是强电解质,完全电离,醋酸是弱电解质,部分电离,故醋酸提供的氢离子比硫酸提供的氢离子多,所以锌与醋酸反应放出的氢气比与硫酸反应放出的氢气多,故不选D。
考点:强弱电解质的比较。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
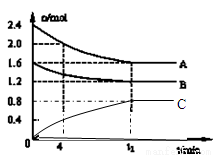
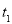 后的某一时刻后,加压,平衡左移,造成这一结果的原因可能是
后的某一时刻后,加压,平衡左移,造成这一结果的原因可能是 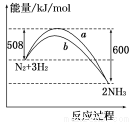
 2NH3 ΔH=-92 kJ/mol
2NH3 ΔH=-92 kJ/mol MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。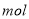 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________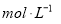 。
。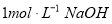 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。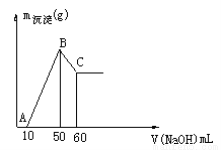
 。
。