题目内容
8.写出下列物质的电子式(1)HF
 (2)KFK+
(2)KFK+
(3)H2O
 (4)Na2S
(4)Na2S
(5)CH4
 (6)CaCl2
(6)CaCl2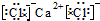 .
.
分析 (1)氟化氢是共价化合物,H原子和F原子间为共价键;
(2)KF为离子化合物,由钾离子和氟离子构成;
(3)水为共价化合物,氧原子最外层8个电子,分子中存在两个氧氢键;
(4)硫化钠中存在钠离子和硫离子,钠离子直接用离子符号表示,硫离子需要标出最外层电子及所带电荷;
(5)CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键;
(6)氯化钙为离子化合物,阴阳离子需要标出电荷,氯离子还要标出最外层电子.
解答 解:(1)氟化氢是共价化合物,H原子和F原子间为共价键,故氟化氢的电子式为 ,故答案为:
,故答案为: ;
;
(2)KF为离子化合物,由钾离子和氟离子构成,故电子式为K+ ,故答案为:K+
,故答案为:K+ ;
;
(3)水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为 ,故答案为:
,故答案为: ;
;
(4)Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子,硫化钠的电子式为: ,
,
故答案为: ;
;
(5)碳原子最外层的4个电子分别与氢原子形成共用电子对,电子式为 ,故答案为:
,故答案为: ;
;
(6)氯化钙为离子化合物,电子式中需要标出阴阳离子所带电荷,氯化钙的电子式为: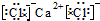 ,
,
故答案为: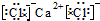 .
.
点评 本题考查了电子式的书写,题目难度不大,注意掌握电子式的概念及书写原则,明确离子化合物与共价化合物的电子式表示方法及区别.

练习册系列答案
相关题目
4.下列装置所示的实验中,能达到实验目的是( )
| A. |  分离碘和酒精 | B. |  除去Cl2中的H Cl碘酒 | ||
| C. |  收集NO | D. |  实验室制取NH3 |
5.在H2S水溶液中,加入一些Na2S固体,将使( )
| A. | H2S解离度增大 | B. | H2S平衡常数减小 | C. | 溶液pH下降 | D. | 溶液pH增大 |
16.下列关于燃烧热的说法正确的是( )
| A. | 1mol纯物质完全燃烧时所放出的热量,叫该物质的燃烧热 | |
| B. | 放热反应热化学方程式中△H就是该反应物的燃烧热 | |
| C. | 物质的燃烧热可利用仪器由实验测得 | |
| D. | 物质燃烧必然伴随发光发热现象且肯定是氧化还原反应 |
3.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O含有的分子数为NA | |
| B. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA | |
| C. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| D. | 常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
13.表第I栏与第II栏中的化学反应,都可以用第III栏中的离子方程式表示的是( )
| 选项 | 第I栏 | 第II栏 | 第Ⅲ栏 |
| A | 往少量NaOH溶液中投入铝片 | 往过量NaOH溶液中 投入铝片 | 2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| B | 往Fe2( SO4)3溶液 中滴入氢氧化钠溶液 | 往Fe2 (SO4)3溶液 中滴入氢氧化钡溶 液 | Fe3++3OH=Fe(OH)3↓ |
| C | NaHCO3溶液滴入Ca(OH)2 | NaHCO3溶液滴入NaOH溶液 | Ca2++OH-+HCO3-=CaCO3↓+H2O |
| D | 往NaOH泪液中通入过量CO2气体 | 往NaOH溶液中通入少量CO2气体 | CO2+OH-=HCO3- |
| A. | A | B. | B | C. | C | D. | D |
20.下列有机化学反应方程式书写及反应类型均正确的是( )
| A. | CH2=CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl 加聚反应 | |
| B. | CH3COOH+CH3CH2OH $?_{△}^{浓H_{2}SO_{4}}$CH3COOCH2CH3+H2O 酯化反应 | |
| C. | 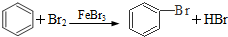 加成反应 加成反应 | |
| D. | 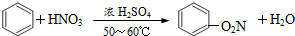 取代反应 取代反应 |
17.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤酯化反应 ⑥加聚反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤酯化反应 ⑥加聚反应.
| A. | ②④ | B. | ①④ | C. | ③⑤ | D. | ②⑥ |
18.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | |
| B. | S(g)+O2(g)=SO2(g);△H1S(s)+O2(g)=SO2(g);△H2 | |
| C. | CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g);△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H2 |