题目内容
15.某含氧物质X仅含三种元素,在如图是常见元素组成的单质或化合物,其中A、B、C为单质,转化关系如下: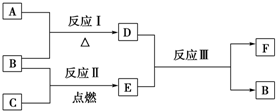
Ⅰ.若B为黄色固体,A为原子半径最小的原子组成的单质.
①反应Ⅲ的化学方程式为2H2S+SO2═3S+2H2O.
②实验测得起始参加反应的B和最后生成的B质量相等,则起始参加反应的A和C的物质的量之比是2:1.
Ⅱ.若D为淡黄色固体化合物,焰色反应为黄色,组成C的元素的原子最外层电子数是内层电子数的2倍.
①D中含有化学键有离子键、共价键.
②写出D与H2O反应的离子方程式2Na2O2+2H2O═4Na++4OH-+O2↑.
③当有7.8g D与H2O反应时转移的电子数为0.1NA.
④反应Ⅲ的化学反应中还原剂与氧化剂的质量比为1:1.
分析 A、B、C为单质,
Ⅰ.若B为黄色固体单质判断为S,A为原子半径最小的原子组成的单质推断为H2,A与B反应生成 D为H2S,根据B、C反应生成 E,E与硫化氢反应生成硫,可知C为O2,E为SO2,硫化氢与二氧化硫反应生成 F为H2O;
Ⅱ.若D为淡黄色固体,焰色反应为黄色,含有钠元素,故D为过氧化钠;组成C的元素的原子最外层电子数是内层电子数的2倍,则C为碳;结合转化关系可知,A为Na、B为氧气、E为二氧化碳、F为碳酸钠,据此解答.
解答 解:A、B、C为单质,
Ⅰ.若B为黄色固体单质判断为S,A为原子半径最小的原子组成的单质推断为H2,A与B反应生成 D为H2S,根据B、C反应生成 E,E与硫化氢反应生成硫,可知C为O2,E为SO2,硫化氢与二氧化硫反应生成 F为H2O,
①反应Ⅲ的化学方程式为,2H2S+SO2═3S+2H2O,故答案为:2H2S+SO2═3S+2H2O;
②发生反应H2+S=H2S,SO2+2H2S=3S+2H2O,S+O2=SO2,由方程式可知二氧化硫与硫化氢为1:2,生成1mol二氧化硫需要1mol氧气,生成2mol硫化氢需要2mol氢气,故参加反应的氢气与氧气的物质的量之比为2:1,
故答案为:2:1;
(2)若D为淡黄色固体,焰色反应为黄色,含有钠元素,故D为过氧化钠;组成C的元素的原子最外层电子数是内层电子数的2倍,则C为碳;结合转化关系可知,A为Na、B为氧气、E为二氧化碳、F为碳酸钠;
①D为过氧化钠,D中含有化学键有离子键、共价键,
故答案为:离子键、共价键;
②D为淡黄色固体,D与H2O反应的离子方程式为2Na2O2+2H2O═4Na++4OH-+O2↑,
故答案为:2Na2O2+2H2O═4Na++4OH-+O2↑;
③过氧化钠与水反应时,每摩尔过氧化钠要转移1mol电子,所以当有7.8g0.1mol Na2O2与H2O反应时转移的电子数为0.1NA,
故答案为:0.1NA;
④反应Ⅲ为2Na2O2+2CO2=2Na2CO3+O2,反应中过氧化钠既是氧化剂又是还原剂,还原剂与氧化剂的质量比为1:1,
故答案为:1:1.
点评 本题考查元素周期表与周期律的综合应用、无机物推断、常用化学用语、电解原理、元素化合物性质等,难度不大,掌握元素周期表的结构推断元素是关键,注意基础知识的理解掌握.

| A. | 往原溶液中加100mL水 | B. | 再加100mL原溶液 | ||
| C. | 将原溶液稀释为200mL | D. | 加入等浓度等体积的硫酸 |
| A. | 硅胶可以用作干燥剂、催化剂 | |
| B. | 为加快漂白粉的漂白速率,可加氢氧化钠 | |
| C. | 氯化铁水解可以制备胶体,所以常用于杀菌消毒 | |
| D. | 淀粉和水可以检验出食盐中含碘 |
| A. | 苯不溶于水,密度比水大 | |
| B. | 苯不能发生氧化反应 | |
| C. | 除去苯中混有的少量甲苯,可以用酸性高锰酸钾溶液 | |
| D. | 苯可以跟溴水反应制取溴苯 |
| A. | 硫离子:S-1 | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 氢氧根的电子式: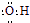 | |
| D. | HClO的结构式:H-O-Cl |
| A. | 该反应的还原剂只有FeSO4 | |
| B. | 每生成1mol Na2FeO4只转移5mol的电子 | |
| C. | K2FeO4作为水处理剂时仅起杀菌消毒的作用 | |
| D. | 该反应在水溶液中进行并不影响高铁酸钾的生产 |
| A. | 水的三态变化--分子的间隔和排列方式发生了改变 | |
| B. | 闻到远处饭菜的香味--分子在不断的运动 | |
| C. | 水通电分解--分子在化学变化中可以再分 | |
| D. | 夏天钢轨之间的缝隙变小--原子受热时体积变大 |
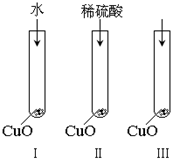 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.