题目内容
16.(1)铜在潮湿的空气中会被锈蚀,表面生成绿色的碱式碳酸铜,写出其化学方程式2Cu+O2+H2O+CO2═Cu2(OH)2CO3.(2)高温下,将CO通入CuO中,现象:黑色粉末变为红色固体,方程式为CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
分析 (1)铜在空气中与O2、CO2、H2O反应产生Cu2(OH)2CO3;
(2)高温下CO具有强还原性,CuO被还原成Cu单质.
解答 解:(1)铜在潮湿的空气中会被锈蚀,生成绿色的碱式碳酸铜,是因为铜在空气中与O2、CO2、H2O反应产生Cu2(OH)2CO3;反应方程式为:2Cu+O2+H2O+CO2═Cu2(OH)2CO3,
故答案为:绿色;碱式碳酸铜;2Cu+O2+H2O+CO2═Cu2(OH)2CO3;
(2)高温下CO具有强还原性,黑色粉末CuO被还原成Cu单质,铜是红色固体,反应方程式为:CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2,
故答案为:黑色粉末变为红色固体;CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2.
点评 本题考查铜及其化合物的性质,属于基础知识的考查,注意碱式碳酸铜化学式的书写,题目比较简单.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
20.下列各项中表达正确的是( )
| A. | 硫离子:S-1 | |
| B. | 用电子式表示氯化氢分子的形成过程: | |
| C. | 氢氧根的电子式: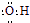 | |
| D. | HClO的结构式:H-O-Cl |
1.某化学兴趣小组学习酸碱中和反应后,对稀盐酸与氢氧化钠溶液混合后的有关问题,进行了如下探究,请你一起参与他们的探究.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
写出其中的方程式:Na2CO3+CuSO4+H2O=CO2↑+Cu(OH)2↓+Na2SO4.
【提出问题】氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
【作出猜想】
甲同学猜想:溶质有NaCl、HCl、NaOH
乙同学猜想:溶质只有NaCl
丙同学猜想:溶质有NaCl、HCl
你的猜想:溶质有NaCl和NaOH.(填化学式)
乙同学认为甲同学的猜想是错误的,理由是由于氢氧化钠可以和稀盐酸反应,所以盐酸和氢氧化钠不能共存.
【实验设计及验证】请你将下列实验报告填写完整:
| 实验操作 | 实验现象 | 实验结论 |
| 取反应后的溶液于试管中,加入碳酸钠溶液 | 紫色石蕊溶液变红色 | 丙同学的猜想正确 |
| 取反应后的溶液于试管中,硫酸铜溶液 | 有蓝色沉淀生成 | 你的猜想正确 |
4.已知:Ksp(AgCl)=1.8×10-10,Ksp(AgBr)=7.8×10-13.现将AgCl与AgBr的饱和溶液等体积混合,再加入足量浓AgNO3溶液,发生的反应为( )
| A. | 只有AgBr沉淀 | |
| B. | AgCl和AgBr沉淀等量生成 | |
| C. | AgCl和AgBr沉淀都有,但以AgCl沉淀为主 | |
| D. | AgCl和AgBr沉淀都有,但以AgBr沉淀为主 |
1.某温度下,Fe(OH)2和Cu(OH)2沉淀溶解平衡曲线如图所示,下列有关说法正确的是( )
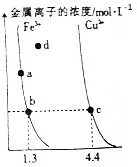

| A. | Ksp[Fe(OH)3]<Ksp[Cu(OH)2] | |
| B. | a、b、c、d四点的Kw不同 | |
| C. | 在Fe(OH)3饱和溶液中加入适量硝酸钾晶体可使a点变到b点 | |
| D. | d点时的Cu(OH)2溶液为不饱和溶液 |
8.只用一种试剂即可鉴别C2H5OH、C6H5OH、AgNO3、Na2CO3、KI五种无色透明溶液,这种试剂是( )
| A. | 稀盐酸 | B. | 稀NaOH溶液 | ||
| C. | FeCl3溶液 | D. | 酸性高锰酸钾溶液 |
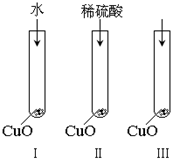 氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.
氧化铜是一种黑色固体,可溶于稀硫酸.某同学想知道是稀硫酸中的哪种粒子(H2O,H+,SO42-)能使氧化铜溶解.请你和他一起通过如图Ⅰ、Ⅱ和Ⅲ三个实验完成这次探究活动.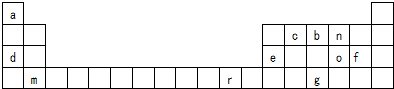
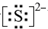 ;化合物ba3的结构式为
;化合物ba3的结构式为 .
.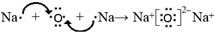 ;
;