题目内容
7.下列关于氨气的说法中正确的是( )
| A. | 氨气溶于水显碱性,所以氨气可以使湿润的酚酞试纸变蓝 | |
| B. | 氨气可以用浓硫酸干燥 | |
| C. | 用水吸收氨气可用如图的装置防止倒吸 | |
| D. | 氨气本身没有毒,因此氨气泄漏时,人们没有必要采取任何防范措施 |
分析 A、氨气能使湿润的酚酞试纸变红;
B、氨气与浓硫酸反应生成硫酸铵;
C、四氯化碳的密度比水大,所以通下层;
D、氨气有刺激性气味.
解答 解:A、氨气能使湿润的酚酞试纸变红,而不是变蓝,故A错误;
B、氨气与浓硫酸反应生成硫酸铵,所以不能用浓硫酸干燥氨气,故B错误;
C、氨气在水中的溶解度大,而在四氯化碳中溶解度小,四氯化碳的密度比水大,所以通下层,防止倒吸,故C正确;
D、氨气有刺激性气味,所以氨气泄漏时,人们必须采取任何防范措施,故D错误;
故选C.
点评 本题考查氨气的检验,侧重元素化合物性质的考查,把握氨气的性质为解答的关键,注意氨水溶液显碱性及反应中的现象,题目难度不大.

练习册系列答案
相关题目
17.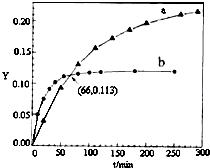 已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
 已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )
已知反应:2CH3COCH3(l)?CH3COCH2COH(CH3)2(l).取等量CH3COCH3,分别在0℃和20℃下,测得其转化分数随时间变化的关系曲线(Y-t)如图所示.下列说法不正确的是( )| A. | b代表20℃下CH3COCH3的Y-t曲线 | |
| B. | 从Y=0到Y=0.113,CH3COCH2COH(CH3)2的$\frac{△n(0℃)}{△n(20℃)}$=1 | |
| C. | 升高温度可缩短反应达平衡的时间并能提高平衡转化率 | |
| D. | 反应进行到20min末,CH3COCH3的$\frac{v(0℃)}{v(20℃)}$<1 |
18.下列关于实验现象的描述不正确的是( )
| A. | 把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面会出现气泡 | |
| B. | 用银片做阳极,铁片做阴极,电解硝酸银溶液,铁片表面会镀上一层银 | |
| C. | 把锌粒放入盛有稀硫酸的试管中,同时加入几滴硫酸铜溶液,气泡放出速率会加快 | |
| D. | 把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
15.下列物质中含有离子键的是( )
| A. | H2O | B. | MgCl2 | C. | CO2 | D. | N2 |
2.下列过程中需要吸收热量的是( )
| A. | 大理石的分解反应 | B. | 氢气燃烧 | ||
| C. | 氧化钙投入水中 | D. | 盐酸与氢氧化钠反应 |
12.下列说法正确的是( )
| A. | 周期表中金属与非金属交界处可找到合成催化剂的元素 | |
| B. | 有热量放出的变化一定是放热反应 | |
| C. | 化学反应中能量变化的主要原因是有化学键的断裂与形成 | |
| D. | 影响化学反应速率的本质因素是催化剂 |
19.已知2H→H2放出437.6kJ的热量,下列说法正确的是( )
| A. | 氢气分子内每个氢原子都达到了8电子稳定结构 | |
| B. | 1molH2的能量比2molH的能量低 | |
| C. | 1molH2离解成2molH要放出437.6kJ的热量 | |
| D. | 氢原子不如氢气分子活泼 |
17.已知1mol CH4气体完全燃烧生成气态CO2和液态H2O,放出890.3kJ热量,则表示该反应的热化学方程式正确的是( )
| A. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=+890.3 kJ•mol-1 | |
| B. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=+890.3 kJ•mol-1 | |
| D. | CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 |
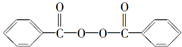
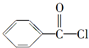 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式: ,该反应属于取代反应.
,该反应属于取代反应.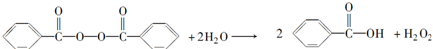 .苯甲酸的同分异构体中,含苯环且属于酯类的结构简式为
.苯甲酸的同分异构体中,含苯环且属于酯类的结构简式为 ,属于酚类结构的同分异构体有3种.
,属于酚类结构的同分异构体有3种.