题目内容
3.常温下将0.1mol的Cl2通入0.5L的水中(不计溶液体积变化),制得氯水,关于这份氯水下列说法正确的是( )| A. | 若不考虑HClO和H20的电离,该溶液中H+的浓度为0.1mol/L | |
| B. | 若在该溶液中加入足量Na0H,则可得到0.1mol的NaClO | |
| C. | 若将此溶液在强光下光照,产生气泡,则气泡主要成分是O2 | |
| D. | 此溶液久置后,由于HClO的大量分解,会导致其pH值升高 |
分析 常温下将0.1mol的Cl2通入0.5L的水中(不计溶液体积变化),制得氯水,发生反应:Cl2+H2O?HCl+HClO,然后滴加NaOH,发生反应:HCl+NaOH═NaCl+H2O、HClO+NaOH═NaClO+H2O,
A.该反应为可逆反应;
B.NaClO为强碱弱酸盐;
C.次氯酸不稳定性,在光照条件下发生:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2;
D.由于HClO的分解导致了Cl2的不断反应,最后变成了HCl溶液,弱酸变成强酸,溶液酸性增强.
解答 解:常温下将0.1mol的Cl2通入0.5L的水中(不计溶液体积变化),制得氯水,发生反应:Cl2+H2O?HCl+HClO,
A.该反应为可逆反应,生成的HCl的物质的量小于0.1mol,若不考虑HClO和H20的电离,该溶液中H+的浓度为小于0.2mol/L,故A错误;
B.NaClO为强碱弱酸盐,发生水解,所以生成的NaClO的物质的量小于0.1mol,故B错误;
C.若将此溶液在强光下光照,发生反应:2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑,则气泡主要成分是O2,故C正确;
D.此溶液久置后,由于HClO的分解导致了Cl2的不断反应,最后变成了HCl溶液,弱酸变成强酸,溶液酸性增强,会导致其pH值减小,故D错误;
故选C.
点评 本题综合考查氯气的性质,题目难度中等,明确溶液中的溶质及其性质是解本题关键,注意盐类水解原理的应用方法.

练习册系列答案
相关题目
13.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 气态氢化物的稳定性:W>Z | |
| D. | W的单质能与水反应,生成一种具有漂白性的物质 |
14.燃烧1g乙醇(液态)生成CO2气体和液态水放出热量为29.7KJ,则乙醇燃烧的热化学方程式正确的是( )
| A. | C2H 5OH+3O2═2CO2+3H 2O△H=-29.7 kJ/mol -1 | |
| B. | C2H 5OH(l)+3O2 (g)═2CO2 (g)+3H 2 O(l)△H=+1366.2kJ/mol -1 | |
| C. | C 2 H 5 OH(l)+3O2 (g)═2CO2 (g)+3H 2O(g)△H=+29.7 kJ/mol-1 | |
| D. | C2H 5OH(l)+3O2 (g)═2CO 2 (g)+3H 2 O(l)△H=-1366.2kJ/mol -1 |
8.下列化学式能代表一种纯净物的是( )
| A. | C3H8 | B. | C4H10 | C. | C5H12 | D. | C2H4Br2 |
15.实验室中,用20mL浓度为3mol/L的稀硫酸与过量的锌粒反应,在一定温度下发生反应制取氢气,为了降低反应速率,但又不影响生成氢气的总量,下列措施能达到目的是( )
| A. | 向稀硫酸中加硫酸钾溶液 | B. | 将锌粒制成薄锌片 | ||
| C. | 向稀硫酸中加碳酸钠固体 | D. | 向稀硫酸中加硝酸钾溶液 |
12.W、X、Y、Z是中学化学常见的四种均含10个电子的微粒,它们之间的转化关系如下.下列叙述错误的是( )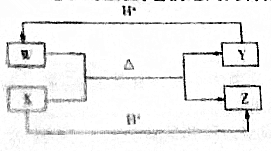

| A. | W的电子式为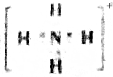 | |
| B. | Y与Z之间可形成氢键 | |
| C. | 硫酸与氢氧化钠溶液反应的离子方程式可表示为X+H+=Z | |
| D. | 微粒Y中各元素原子均达到8电子稳定结构 |
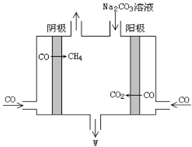 (1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O.
(1)利用CO2与H2反应可合成二甲醚(CH3OCH3).以KOH为电解质溶液,组成二甲醚--空气燃料电池,该电池工作时其负极反应式是CH3OCH3-12e-+16OH-=2CO32-+11H2O. ,形成过程
,形成过程 ;
;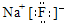 ,形成过程
,形成过程 ;
; ,形成过程
,形成过程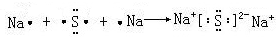 ;
; ;
; ,形成过程
,形成过程 .
.