题目内容
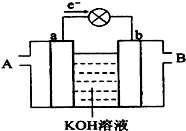 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气4.48 L |
考点:化学电源新型电池
专题:电化学专题
分析:A.燃料电池中,通入燃料的电极失电子、通入氧化剂的电极得电子;
B.a电极上CO和氢气失电子发生氧化反应;
C.a电极发生氧化反应、b电极发生还原反应;
D.根据转移电子相等进行计算.
B.a电极上CO和氢气失电子发生氧化反应;
C.a电极发生氧化反应、b电极发生还原反应;
D.根据转移电子相等进行计算.
解答:
解:A.电子的流向可知,电子从a极出来,回到b极,所以a是负极(燃料失电子),b极是正极(O2得电子),故A错误;
B.在负极上CO和H2失电子,CO失电子后变成+4价(以CO2形式存在),而电解质溶液是碱性溶液,所以CO2会与OH-发生反应生成CO32-,故a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O,故B正确;
C.a电极是负极,发生氧化反应,b电极是正极,得到电子,发生还原反应,故C错误;
D.如用这种电池电镀铜,当镀件增重6.4gCu,说明n(Cu)=0.1mol.转移n(e-)=0.2mol,1molCO转移2mol e-,1mol H2转移2mol e-,1molCO和H2的混合气体也是转移2mol e-,现增重6.4gCu,转移0.2mol e-,所以消耗CO 0.1mol或0.1mol H2或CO和H2的混合气体0.1mol,则消耗标准状况下的水煤气2.24 L,故D错误;
故选B.
B.在负极上CO和H2失电子,CO失电子后变成+4价(以CO2形式存在),而电解质溶液是碱性溶液,所以CO2会与OH-发生反应生成CO32-,故a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O,故B正确;
C.a电极是负极,发生氧化反应,b电极是正极,得到电子,发生还原反应,故C错误;
D.如用这种电池电镀铜,当镀件增重6.4gCu,说明n(Cu)=0.1mol.转移n(e-)=0.2mol,1molCO转移2mol e-,1mol H2转移2mol e-,1molCO和H2的混合气体也是转移2mol e-,现增重6.4gCu,转移0.2mol e-,所以消耗CO 0.1mol或0.1mol H2或CO和H2的混合气体0.1mol,则消耗标准状况下的水煤气2.24 L,故D错误;
故选B.
点评:本题考查原电池的工作原理及应用,明确电极反应的判断和电极反应式的书写即可解答,注意电子守恒在计算中的应用,题目难度不大.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、向CaCl2溶液中通入少量CO2气体:Ca2++CO2+H2O=CaCO3↓+2H+ |
| B、将少量二氧化碳通入烧碱溶液中:CO2+OH-=HCO3- |
| C、向Ba(OH)2溶液中滴加NaHSO4溶液至刚好沉淀完全:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| D、NaHCO3溶液与NaHSO4溶液混合:HCO3-+H+=H2O+CO2↑ |
 已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )(提示:KspAgCl>KspAgI)
已知:pAg=-lg{c(Ag+)},KspAgCl=1×10-12如图是向10mLAgNO3溶液中逐渐加入0.1mol/L的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是( )(提示:KspAgCl>KspAgI)| A、原AgNO3溶液的物质的量浓度为0.1 mol?L-1 |
| B、图中x点的坐标为(10,6 ) |
| C、图中x点表示溶液中Ag+ 与Cl-浓度相同 |
| D、把0.1 mol?L-1的NaCl换成0.1 mol?L-1NaI则图象在终点后变为虚线部分 |
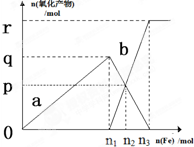 含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )
含有4.0mol HNO3的稀硝酸分别与不同质量的铁粉反应,所得氧化产物a、b与铁粉物质的量关系如图所示(还原产物只有NO).下列有关判断正确的是( )| A、a是Fe(NO3)2 |
| B、n1=0.80 |
| C、p=0.60 |
| D、n3=1.20 |
下列实验操作中,错误的是( )
| A、分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| B、配制90mL1mol/L的NaOH溶液选用100 mL容量瓶 |
| C、用pH试纸测得新制氯水的pH为2 |
| D、用酸式滴定管准确量取10.00mLKMnO4溶液 |